Betalaini
Autor: Stana Mićović, dipl. ing.
Recezent: prof. dr Biserka Vujičić
.
.
Betalaini su grupa pigmenata koji u molekulu sadrže azot, koji mogu biti žute, narandžaste, ružičaste (pink), crvene i purpurne boje. Za razliku od ostale tri grupe biljnih pigmenata (hlorofil, karotenoidi i flavanoidi), betalaini imaju ograničenu rasprostranjenost. Većina crvenog obojenja kod biljaka potiče od karotenoida i flavonoida. Betalaini su ograničeni na biljke iz reda Caryophylales i gljive Amanita. Pored Beta vulgaris (familija Chenopodiaceae), betalaini su opisani kod plodova Cactaceae (prickly pear, „bodljikava kruška“), semenu Amarant-a (Amaranthaceae), delova cveta biljke Bougainvillaea (Nyctaginaceae), cvetovima ili drugim delovima biljaka iz Aizoaceae, Basellaceae, Didieraceae, Phytolaccaceae i Portulaceae. Devet od jedanaest familija iz reda Caryophyllales imaju biljke koje sadrže betalaine. Ostale dve familije (Caryophyllaceae i Molluginaceae) imaju antocijane (flavonoide), što se verovatno odražava na ranu taksonomsku podelu u ovom biljnom redu. Cvekla i „bodljikava kruška“ (Opuntia ficusindica) su jedini jestivi izvori betalaina (Nottingham, 2004). Betalaini se nalaze u različitim biljnim organima i akumulirani su u ćelijskim vakuolama, uglavnom u epidermalnim i subepidermalnim tkivima. Međutim, ponekad su akumulirani u biljnim stabljikama, kao što su podzemni delovi cvekle, semenu (Bougainvilles spp.), cveću i lišću (Delgado-Vargas et al., 2000).
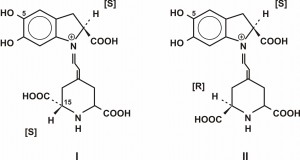
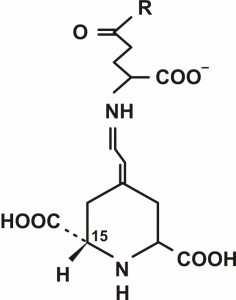
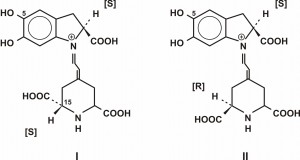
Betalaini se mogu podeliti na dve osnovne strukturne grupe: crveno-ljubičaste betacijanine (slika 1) (od latinskog Beta, cvekla, i grčkog kyanos, plava boja) i žute betaksantine (slika 2) (latinski Beta i grčki xanthos, žut). Svaku grupu pigmenata karakteriše specifičani ostatak R1-N-R2. Opisano je više od 50 betalaina, svi su sa istom osnovnom strukturom, a R1 i R2 grupe mogu biti vodonik, aromatična grupa ili drugi supstituent (Tabela 5). Boja betalaina pripisuje se rezonantnim dvostrukim vezama .Kada se osnovna struktura supstituiše aromatičnim jezgrom, zapaža se promena apsorpcionog maksimuma sa 540 nm (crveno-purpurni betacijanini kao što je betanidin) na 480 nm (žuti betaksantini kao što je miraksantin-II). Konjugacijom sa nekoliko amino jedinjenja kao što su amino kiseline može se formirati veliki broj betaksantina, sa istim dihidropiridinskim ostatkom; kao na primer, R2 grupa vulgaksantina-I iz B. Vulgaris dobija se iz glutaminske kiseline. S druge strane, raznolikost betacijanina povezana je sa kombinacijom osnovnih struktura (betacijanin je najvažniji zatim izobetanidin, njegov C15 epimer) sa različitim glikozil i acil grupama vezanih za hidroksi grupu na položajima 5 i 6.
.
Betalaini su dobili ime prema biljci iz koje su prvobitno izolovani: betacijanin amarantin-I iz Amaranthus tricolor, betanin iz Beta vulgaris i gromfrenin-I iz Gomphrena globosa; betaksantini, miraksantin iz cvetova Mirabilis jalapa, vulgaksantin-I i –II iz korena cvekle (B. vulgaris) i portulaksantin iz latica Portulaca grandiflora.
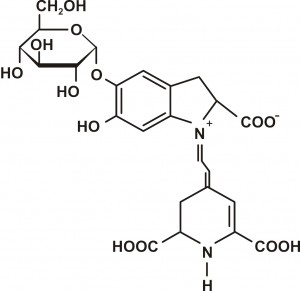
Cvekla sadrži kompleksnu smešu betalain pigmenata. Glavni pigment cvekle je betanin (glikozid betanidina) (slika 3). Betanin je otkriven oko 1920. godine, dok je kristalni oblik betaninske boje proizveden 1960-tih godina. U korenu cvekle se betanin normalno nalazi u mnogo većoj količini u odnosu na ostale betacijaninske pigmente. Kao i svi betacijanini, betanin se metabolički izvodi iz molekula poznatog kao 3,4-dihidroksifenilalanin (L-DOPA). Betanin nastaje iz dva molekula L-DOPA. Jedan molekul podlaže promeni u oblik betalaminske kiseline („betalamic acid“). Drugi molekul L-DOPA menja se u ciklo-DOPA glukozid (CDG), koji se kondenzuje sa betalaminskom kiselinom i gradi betanin. Mala promena u strukturi prevodi betanidin u betanin. Druge male biohemijske modifikacije daju druge betacijaninske pigmente (Nottingham, 2004). Najznačajniji faktori koji utiču na sintezu pigmenata cvekle su temperatura, plodnost zemlje, vlažnost zemlje, navodnjavanje i vreme berbe (vađenja).
Tabela 5. Primeri betalaina (Jackman & Smith 1996., i Delgado-Vargas et al. 2000)
| Betacijanini | |||
| Naziv | R1 | R2 | Botaničko nalaženje |
| Betanin | β-glukoza | H | Beta vulgaris |
| Filokaktin | 6′-O-(malonil)-β-glukoza | H | Phyllocactus Hybridus |
| Lamparantin I | 2′-O-p-kumaroil-β-glukoza | H | Lamparanthus spp. |
| Amarantin | 2′-O-(β-glukoronska kiselina)-b-glukoza | H | Amaranthus tricolor |
| Celozijanin-II | 2′-O-[-O-(trans-feruloil)-β-glukuronska kiselina]-β-glukoza |
H | Celosia cristata L. |
| Betaksantini | |||
| Naziv | R1 | R2 | Botaničko nalaženje |
| Indikaksantin | obe grupe zajedno iz prolina | obe grupe zajedno iz prolina | Opuntia ficus-indica |
| Portulakaksantin-I | obe grupe zajedno iz hidroksiprolina | obe grupe zajedno iz hidroksiprolina | Porulaca grandiflora |
| Vulgaksantin-I | H | Glutamin | Beta vulgaris |
| Vulgaksantin-II | H | Glutaminska kiselina | Beta vulgaris |
| Dopaksantin | H | L-DOPA | Glottiphyllium Longum |
R3 i R4 mogu biti acil ili glikozil supstituentske grupe
.
.
Posle betanina, žuti betaksantini, vulgaksantin-I i vulgaksantin-II su najznačajniji pigmenti cvekle. Ove pigmente su prvi opisali Mario Piattelli sa saradnicima 1960-tih godina u Napulju. U kulturama koje su istraživali (Piatta d’Egitto) pronašli su najmanje šest betaksantina, koji su svi bili u minornim količinama. Ukupno, naveli su šesnaest različitih betalaina, uključujući indikaksantin (indicaxanthin), izobetanin (isobetanin), neobetanin i prebetanin. Karakteristična boja korena cvekle je posledica varijacija različitih betalainskih pigmenata, pogotovo relativnih koncentracija betanina i žutih betaksantina. Vrste sa tamno purpurno-crvenom bojom imaju visok odnos betanina prema betaksantinima, dok žute i zlatne vrste kao što su Burpee’s Golden, imaju relativno veliku količinu betaksantina i veoma malo ili uopšte nemaju betanine. Vrste sa belim korenjem, uključujući Albina Vereduna i Blankoma, imaju ekstremno male količine i betacijanina i betaksantina.
Izrazito tamni i svetli prstenovi obično su vidljivi kada se cvekla poprečno preseče. Ovo je posledica različite količine pigmenata u vaskularnom sistemu i skladišnom tkivu (storage tissue) korena. Vaskularni sistem se vidi kao tamni prstenovi usled velike količine pigmenata, dok skladišno tkivo izgleda kao svetliji prstenovi. Kod nekih tamno crvenih vrsta kao što su Boltardy i Red Ace, ove razlike u boji su jedva primetne. Razlika u boji je najočitija kod vrste Chioggia, sa koncentričnim šarama (kao meta) ružičasto-crvene (vaskularni sistem) i bele boje (skladišno tkivo).
Sadržaj betacijanina u cvekli je (75-95 %) i žutih betaksantina (~95% vulgaksantina I). U spoljnjim delovima cvekle (ljuske) je najveća koncentracija betanina (Kujala et al., 2000) (tabela 6).
Betacijanini su stabilniji od betaksantina na 25oC (Kujala et al., 2002).
Tabela 6. Sadržaj betanina u delovima korena cvekle (mg/g SM) (Kujala et al., 2002)
| Deo biljke | Betanin | Vulgaksantin I i II | Izobetanin |
| Ljuska | 3,8-7,6 | 1,4-4,3 | 1,2-3,1 |
| Meso | 2,9-5,2 | 1,5-4,0 | 0,02-0,4 |
.
Cvekla sadrži ~130 mg betanina/100g sirovine. Nove selekcije mogu sadržavati i do 450-500 mg betanina/100g.
Među betacijanima najzastupljeniji je betanin i najznačajniji. Pored betanina postoje još isobetanin, betanidin i isobetanidin (tabela 7) (Slika 4)
.
.
Betalaini su uglavnom raspoređeni prema spoljnim delovima korena cvekle. Međutim, nisu ograničeni samo na koren, već daju crvenu boju koja se može zapaziti na listovima, stabljici i cvetovima (Nottingham, 2004).
Tabela 7. Vrste betacijanina u cvekli (g/kg) (Gasztonyi et al., 2001)
| Vrsta | Betanin | Isobetanin | Betanidin | Isobetanidin |
| Bonel | 0,50 | O,27 | 0,04 | 0,01 |
| Nero | 0,41 | 0,13 | 0,03 | 0,01 |
| Favorit | 0,49 | 0,24 | 0,05 | 0,02 |
| Rubin | 0,46 | 0,25 | 0,07 | 0,03 |
| Detroit | 0,44 | 0,21 | 0,05 | 0,01 |
.
Tabela 8. Vrste žutih pigmenata u cvekli (g/kg) (Gasztonyi et al., 2001)
| Podtipovi | Vulgaksantin I | Vulgaksantin II |
| Bonel | 0,42 | 0,06 |
| Nero | 0,32 | 0,03 |
| Favorit | 0,41 | 0,03 |
| Rubin | 0,36 | 0,03 |
| Detrit | 0,37 | 0,04 |
.
Od žutih betaksantina najveći procenat čini vulgaksantin I (tabela 8).
Pigmenti cvekle pokazuju atioksidativna svojstva (Kanner et al., 2001; Escribano et al., 1998). U različitim model sistemima je dokazano da su betacijanini jaki antioksidanti. Njihov pozitivan elektrostatički naboj povećava afinitet prema biološkim membranama, koje su glavne mete oksidacije (Kanner et al., 2001).
Prema važećoj zakonskoj regulativi (Sl. list SCG 56/2003 sa izmenama i dopunama 4/2004, 5/2004, 16/2005) u našoj zemlji dozvoljena je primena betanina, kao glavnog pigmenta cvekle, kao prirodne prehrambene boje E162.
Funkcije betalaina
Taksonomski markeri
Betalaini i antocijanini imaju veoma različite strukture i njihova rasprostranjenost jedna drugu isključuje. Proizvodnja betalaina je ograničena na red Caryophyllales i samo dve familije imaju antocijanine umesto betalaina, Caryophyllaceae i Molluginaceae, ukazujući na ranu diferencijaciju ovog reda u grupe sa različitim vrstama pigmenata (Delgado-Vargas, Paredes-López, 2002). Prema tome, primena betalaina kao toksonomskih markera („otisak prsta“ pri sistematizaciji) je opravdana.
.
Ekološki i fiziološki aspekti
Betalaini su prisutni u cveću i plodovima i mogu imati ulogu privlačenja insekata i ptica u procesu oprašivanja ili rasprostiranju semena. Njihovo prisustvo u ostalim strukturama biljaka, kao što je lišće, stablo i koren, nije lako funkcionalno objasniti. Međutim, akumulacija betalaina u cvekli povezana je sa skladištenjem ugljenih hidrata kao fiziološka reakcija pod stresnim uslovima. Betalaini su predloženi kao odbrambeni mehanizam pošto se akumiliraju kada je tkivo oštećeno. Osim toga, njihovo prisustvo se javlja u asocijaciji sa antifugalnim proteinima kod nekih biljaka(Delgado-Vargas, Paredes-López, 2002).
.
Primena i stabilnost betalaina
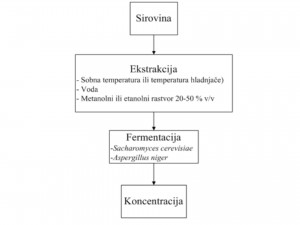
U prehrambenoj industriji betalaini predstavljaju važnu prirodnu boju. Osnovni izvor betalaina je cvekla. Tokom komercijalne ekstrakcije cvekla se prvo usitnjava, obojeni sok se skuplja i koncentriše. Betalaini se prodaju prehrambenoj industriji kao koncentrat soka ili prah. Sok se koncentriše u vakuumu dok se ne dostigne 60-65% ukupne suve materije. U proizvodnji praha (koji obično sadrži 0,3-1,0% pigmenata) se primenjuje liofilizacija (Nottingham, 2004).
U sokovima i praškastim proizvodima visoka koncentracija pigmenata se postiže fermentacijom. Fermentativne materije rastvorljive u soku cvekle mogu se ukloniti u biofermentoru, primenom kvasaca kao što su Candida utilis i Saccharomyces cerevisiae, da bi ostao koncentrovaniji (u odnosu na pigmente) proizvod. Prahovi dobijeni nakon fermentacije soka cvekle sadrže 5-7 puta veću količinu betacijanina od prahova dobijenih iz nefermentisanog soka (Nottingham, 2004).
Ekstrakti betalaina mogu imati široku paletu boja, u zavisnosti od relativnog odnosa prisutnih betacijanina i betaksantina. Proizvodi za bojenje obično su bez mirisa i ukusa, ali mogu uticati na miris i flejvor namirnica. Najvažnije sredstvo za bojenje je čist betanin, E-162 (cvekla crvena), koji se koristi za bojenje širokog opsega prerađenih prehrambenih proizvoda (Nottingham, 2004).
Najveći problem u primeni betalaina u namirnicama je stabilnost, koja ograničava njihovu primenu. Sa ekstraktima betalaina se mora pažljivo manipulisati pošto su osetljivi na uticaje spoljašnje sredine, pogotovo na pH, toplotu, svetlost, vlagu i kiseonik. Uticaji spoljašnje sredine imaju interaktivni uticaj i pigmenti se brzo mogu obezbojiti u nepovoljnim uslovima. Crveni pigment betanin se degradira do svetlo mrke boje pri izlaganju vazduhu, jakoj svetlosti i visokim temperaturama. Ova diskoloracija je delimično reverzibilna, ukoliko su nepovoljni uslovi samo privremeni.
Betalaini ostaju nepromenjeni u pH opsegu od 3,5 do 7,0 (kisela do neutralna sredina). Ekstrakti cvekle u većini namirnica se stoga neće obezbojiti kao direktna posledica pH. Optimalan pH za boju betacijanina i betaksantina je u slabo kiseloj sredini, u opsegu od 5,0-6,0. Boja ekstrakta cvekle menja se iz crvene prema plavoj promenom pH preko 7,0. Tkivo cvekle izloženo visokim ili alkalnim pH (7,5-8,5) postaje obezbojeno. Sečena cvekla dobro zadržava svoju purpurno-crvenu boju u kiselim rastvorima kao što je sirćetna kiselina.
Zagrevanje betalaina može izazvati diskoloraciju. Crveni pigment betanin, na primer, može postati svetlo braon ukoliko se postepeno zagreva, pogotovo ako su povišene temperature udružene sa alkalnim pH.
Stabilnost betalaina je najveća u prehrambenim proizvodima sa niskim sadržajem vlage. Visok nivo vlage povećava brzinu degradacije pigmenata. Tokom vremena, izloženost kiseoniku ubrzava potamnjivanje ili diskoloraciju pigmenata u prehrambenim proizvodima. Betalaini reaguju sa vazdušnim kiseonikom, ali diskoloracija je delimično reverzibilna ukoliko se nivo kiseonika odmah smanji.
Uprkos relativnom nedostatku stabilnosti u poređenju sa sintetičkim prehrambenim bojama, betalaini se široko primenjuju u prehrambenoj industriji (Nottingham, 2004).
Bojene materije cvekle se široko primenjuju zbog svoje stabilnosti u vodenoj sredini. Istraživanja su pokazala (potvrdila) da je betanin termolabilan i da njegova toplotna stabilnost zavisi od pH i kiseonika. Uklanjanje kiseonika povećava njegovu toplotnu stabilnost. Međutim, veoma je teško razjasniti stabilnost pigmenata, pošto enzimska aktivnost, stepen razblaženja, koncentracija kiseonika, vrsta, izloženost svetlosti i priroda pufera utiču na njihovo ponašanje.
Izlaganje rastvora betanina svetlosti na 25oC znatno utiče na njegovu stabilnost, dok je na 55oC degradacija usled toplote toliko izražena, da je izloženost svetlu zanemarljiva. Takođe, degradacija betanina u rastvoru je delimično reverzibilan proces (Pedreno & Escribano, 2001).
Ekspertski tim FAO i WHO preporučuje primenu proizvoda od cvekle u mlečnim proizvodima, svežem voću i povrću, pastama, svežem mesu, svežim jajima, dečjoj hrani, voćnim sokovima, nektarima i vinima itd. (Vargas & Lopez, 2003). Najpogodniji su za primenu u prehrambenim proizvodima koji se podvrgavaju minimalnoj toplotnoj obradi, kratke održivosti, pakovanih u sušenom obliku pod smanjenom količinom kiseonika, svetlosti i vlage.
.
Tabela 9. Stabilnost betalaina u model sistemima (Delgado-Vargas et al., 2000)
| Faktor | Model sistem | Zapažanje |
| pH | Rastvori betalaina | Maksimalna stabilnost boje između pH 3,5 i 7 λmaxbetacijanina: 537-538 nm λmaxbetaksantina: 475-478 nm pH < 3,5, λmax se pomera ka manjim talasnim dužinama, smanjuje se molarna apsorptivnost pH > 7, λmax se pomera ka manjim talasnim dužinama, smanjuje se molarna apsorptivnost |
| pH | Rastvori betalaina sa kiseonikom | Maksimalna stabilnost boje između pH 5,5 i 8 |
| pH | Rastvor cvekle | Maksimalna stabilnost na pH 5,5 |
| pH | Rastvor vulgaksantina | Maksimalna stabilnost između pH 5 i 6 |
| Temperatura | Rastvor betanina | Zagrevanje umanjuje crvenu boju, ali hlađenje može da povrati reakciju; degradacija prati reakciju prvog reda |
| Svetlost | Rastvor betanina | Brzina degradacije betanina se povećava za 15,6% pri izloženosti dnevnom svetlu na 15oC; degradacija prvog reda sa zavisnošću od pH većoj na pH 3 (k = 0,35/dan) nego na pH 5 (k = 0,11/dan) po fluorescentnim svetlom Potpuna razgradnja pigmenata UV zračenjem ili gama zračenjem |
| Aktivitet vode | Betanin u različitim model sistemima |
Nizak aw povećava stabilnost betalaina; stabilnost se smanjuje za jedan red veličina kada aw poraste sa 0,32 na 0,75 |
| Kiseonik | Rastvor betanina | Na pH 7,0 razgradnja betanina je 15% veća u prisustvu vazduha nego u atmosferi azota |
.
.
Najsofisticiranija savremena metoda razdvajanja i kvantifikacije betalaina je visokopritisna tečna hromatografija (HPLC). U tabeli 10 prikazane su metode razdvajanja i prečišćavanja betalaina. Ispitivanjima su zabeležene razlike između spektrofotometrijskih i HPLC metoda. Istraživanja su pokazala da je kvantifikacija betalaina kapilarnom elektroforezom u bliskoj saglasnosti sa HPLC određivanjem.
Tabela 10. Metode razdvajanja i prečišćavanja u izučavanju betalaina (Delgado-Vargas et al., 2000)
| Metodologija | Osobine |
| Elektroforeza | Čvrst nosač: papir Rastvarač: piridin, mravlja ili sirćetna kiselina Voltaža: 5,6 V/cm |
| Kapilarna elektroforeza | Čvrst nosač: tečni silika gel Voltaža: 22kV Temperatura: 18oC Razdvajanje izomernih oblika kao što su betanin i izobetanin, kao i aglikoni |
| Tankoslojna hromatografija (TLC) | Čvrst nosač: ploče presvučene celulozom Rastvarači: izopropanol-etanol-voda-sirćetna kiselina 6:7:6:1 v/v i 11:4:4:1 v/v Kiselina olakšava separaciju pošto protonovani betalaini imaju veću mobilnost Čvrst nosač: dietilaminoetil celuloza Rastvarač: izopropanol-voda-sirćetna kiselina 13:4:1 v/v Dobro razdvajanje betaksantina |
| Jonoizmenjivačka hromatografija | Čvrst nosač:Domex, 50W-X2, Merek I, DEAE-Sephadex i A-25, između ostalog |
| Visokopritisna tečna hromatografija (HPLC) |
Čvrst nosač: obrnute faze C8 ili C18 (NucleosilTM, LiChrosorbTM, μBondapackTM, između ostalih kolona) Rastvarači: voda-metanol, voda-acetonitril Smeše su zakišeljene sirćetnom, mravljom ili fosfornom kiselinom |
.
Karakterizacija
Postoji nekoliko hemijskih testova za razlikovanje (prepoznavanje) antocijana od betalaina, koji su navedeni u tabeli 11.
U cilju karakterizacije betalaina, mogu se primeniti još neka važna određivanja (tabela 12). Betalaini, kao pigmenti, imaju maksimum apsorbancije u vidljivom delom spektra, što ih karakteriše; jasno je da se strukturne modifikacije mogu pratiti primenom UV-VIS spektroskopije. Acetilovani betalaini pokazuju drugi (sekundrani) maksimum apssorbancije u UV delu spektra od 260 do 320 nm i odnos maksimuma u vidljivom spektru prema maksimumu u UV spektru koristi se kao merilo broja acil grupa u strukturi. Osim toga, kvantifikacija pigmenata izučava se primenom matematičkih metoda povezanih sa UV/VIS spektroskopijom. Usavršavanjem metodološkog pristupa se HPLC metoda može povezati sa DAD, MS i NMR. Na taj način, separacija i identifikacija mogu da se izvode simultano. Osim toga, uvedeno je nekoliko hemijskih testova za karakterizaciju betalaina, i veliki broj njih zasniva se na promenama pH vrednosti(Delgado-Vargas & Paredes-López, 2002).
Tabela 11. Razlikovanje antocijana od betalaina (Piatelli, 1981., i Strack et al., 1993)
| Test | Antocijani | Betalaini |
| Dodatak KOH, NaOH | Konačna boja se menja u plavo-zelenu | Boja se menja u žutu |
| Elektroforeza | Kretanje ka katodi | Kretanje prema anodi |
| Dodatak vrelog vodenog rastvora HCl | Stabilna boja | Destrukcija boje |
| Estrakcija amil alkoholom | Da, pri niskim pH | Ne započinje ni pri kojoj vrednosti pH |
| Tankoslojna hromatografija: n-butanol-sirćetna kiselina-voda (BAW) vodeni rastvori |
Umerena mobilnost | Ne |
| Kolonska hromatografija katjonske smole | Niska/srednja mobilnost Elucija vodom | Velika mobilnost Elucija smešom metanol/HCl |
.
Tabela 12. Hemijski testovi i testovi karakterizacije u cilju izučavanja strukture betalaina (Delgado-Vargas et al. 2000)
| Metoda | Procenjena osobina |
| Spektroskopija | Crveno-ljubičasti betacijanini: λmax=540 nm Žuti betaksantini: λmax=480 nm |
| Hidroliza betacijanina | Kiselina: razblaženim vodenim rastvorom HCl; dobija se smeša aglikona u oba izomerna oblika, 15R i 15S epimeri Enzimski: dobija se samo 15S izomer |
| Hidroliza betaksantina | Vodenim rastvorom 1N HCl ili 0,6N amonijakom: dobija se betalaminska kiselina i slobodne amino kiseline |
| Zagrevanje | Betanin se razlaže na betalaminsku kiselinu i ciklo-DOPA 5-O-glukozid |
| Alkalna fuzija | Betanin se cepa na 4-metilpiridin-2,6-dikarbonsku kiselinu i mravlju kiselinu; metoda se primenjuje za otkrivanje „carbon structure“: od betanidina sa stvara betanin-izobetanin u odnosu 3:2, dok je kod izobetanina odnos 2:3 |
| Sinteza betanina | Betanin se u rastvoru 0,6N amonijaka meša sa amino kiselinom10M; ukoliko je amino kiselina glutaminska kiselina, tada je vulgaksantin-II betaksantin |
| Stvaranje neoderivata | Betanin se meša sa diazometanom u metanolnom rastvoru u cilju stvaranja odgovarajućih metil estara |
| Boja | Određuje se tristimulusnom kolorimetrijom; kod cvekle, vrednost b mogu se koristiti za procenu odnosa betaksantin-betacijanin |
DOPA=5,6-dihidroksifenilalanin
.
Tabela 13. Primena betanina u prehrambenoj industriji (JEFCA, 2001)
| Namirnica | Maksimalna količina |
| Mlečni proizvodi | GMP |
| Masti i ulja bez vode | GMP |
| Površinski tretirano sveže voće i povrće | GMP |
| sušene paste i nudle i slični proizvodi | GMP |
| Sveže meso, živinsko meso i divljač; celi ili sčeni delovi | GMP |
| Sveže meso, živinsko meso i divljač | 100 mg/kg |
| Morski proizvodi (riba, mekušci i ljuskari između ostalog) | GMP |
| Sveža jaja | GMP |
| „Infant formulae and follow-on formula“ | GMP |
| Hrana za odvikavanje od sisanja za bebe i decu koja rastu | GMP |
| Voćni sokovi i nektari | GMP |
| Vina | GMP |
GMP = Good Manufacturing Practice (dobra proizvođačka praksa)
.
Literatura
Journal of Agricultural and Food Chemistry.Journal of Agricultural and Food Chemistry
Natural colorants for food and nutraceutical uses
Characterization of the antiradical activity of betalains from Beta vulgaris L. roots
Chemistry, Biochemistry, and Dietary Role of Potato Polyphenols. A.Journal of Agricultural and Food Chemistry
Antioxidant Activity of Plant Extracts Containing Phenolic Compounds.Journal of Agricultural and Food Chemistry
BetalainsA New Class of Dietary Cationized Antioxidants.Journal of Agricultural and Food Chemistry
Phenolics and Betacyanins in Red Beetroot (Beta vulgaris) Root: Distribution and Effect of Cold Storage on the Content of Total Phenolics and Three Individual Compounds.Journal of Agricultural and Food Chemistry
Betalains and phenolics in red beetroot (Beta vulgaris) peel extracts: extraction and characterization
Antioxidsnt content of whole grain breakfast cereals, fruits and vegetable. Journal of American College of Nutrition.Journal of American College of Nutrition
Comparison of red beet (Beta vulgaris var condiva) varieties on the basis of their pigment components
Correlation between antiradical activity and stability of betanine from Beta vulgaris L. roots under different pH, temerature and light conditions. Journal of the Science of Food and Agriculture
An industrial approach in the search of natural antioxidants from vegetable and fruit wastes. Food Chemistry
Effect of processing conditions on soluble sugars content of carrot, beetroot and turnip. Food Chemistry
By-products of plant food processing as a source of functional compounds-recent developments. Trends in Food Science & Technology
Anthocyanins and betalains. Natural Colorants for Food and Nutraceuttical Uses
Phenol antioxidant quantity and quality in foods: vegetables. Journal of Agricultural and Food Chemistry
Comparison of two methods of fiber analysis of 58 foods. Journal of Food Composition and Analysis
Betalains, Current Protocols in Food Analytical Chemistry
Determination of total phenolics, Current Protocols in Food Analytical Chemistry
Radical scavenging and antimicrobial activity of horsetail (Equisetum arvense L.) extracts. Journal of Food Science and Tehnology
Pravilnik o kvalitetu i uslovima upotrebe aditiva u namirnicama i o drugim zahtevima za aditive i njihove mešavine (Službeni list SCG, 56/2003 sa izmenama i dopunama 4/2004, 5/2004, 16/2005)