Autor: dipl. ing. Gordana Koprivica
Mentor: Prof. dr Spasenija Milanović
.
.
Uvod
Uticaj sadržaja vode u hrani na njenu kvarljivost poznat je još od davnina. Između 15000. i 10000. godine p.n.e. naši preci počeli su čuvati višak ribe, mesa i voća sušenjem na vetru i suncu (Ray, 1992). Oko 8000. godine p.n.e. predstavljene su mnoge inovacije u metodama očuvanja hrane. Da bi se obezbedila stalna zaliha hrane, žitarice i voće su bili stabilizovani prirodnim sušenjem a višak mesa i ribe su se štitili dimljenjem i suvim soljenjem. Masson i Challet su 1795. godine primenili veštačko sušenje povrća u zagrejanoj prostoriji. U 20-om veku, inovacije su obuhvatale veštačko sušenje tečnosti primenom metoda sušenja na valjcima i raspršivanjem kao i sušenje smrzavanjem.
Metode konzervisanja hrane sušenjem i soljenjem, razvijane nekoliko milenijuma, bile su empirijske i više kao jedna umetnost nego nauka.
Prilično interesovanje za uticaj aktivnosti vode (aw) na kvalitet i stabilnost prehrambenih proizvoda počelo je u ranim 1950-im (Scott, 1953. i 1957. ). Ono je bilo izazvano empirijskim i protivurečnim opažanjima između ukupnog sadržaja vlage i stabilnosti proizvoda. Nasuprot tome, izmerena vrednost aktivnosti vode (aw) je, uopšteno, u dobrom uzajamnom odnosu sa potencijalom za rast i metaboličku aktivnost pa je usvojena kao dobar indikator prisustva vode za mikrobiološku aktivnost (Christian, 2000; Chirife, 1995; Lenovich, 1987).
Kao rezultat rada, u poslednjih nekoliko godina, kontrola aw vrednosti je uključena u različite zakonske regulative, uzimajući u obzir da aktivnost vode više nego ukupan sadržaj vlage, utiče na rast, smrt, opstanak, sporulaciju i proizvodnju toksina od strane različitih mikroorganizama kao i na podešavanje graničnih aw vrednosti u prehrambenim proizvodima.
Od svih faktora koji utiču na mikrobiološki rast, smrt i opstanak u hrani, uticaj aw na vegetativne mikroorganizme i spore je jedan od onih koji su najviše proučavani od strane prehrambenih mikrobiologa.
.
Osmoanabioza
Namirnice se veoma često konzervišu postupcima koji imaju za cilj da se u njima poveća osmotski pritisak.
Razdvajanjem rastvarača i rastvora neke supstance polupropustljivom membranom javlja se težnja za izjednačavanjem njihovih koncentracija. Kada membrana nije prisutna, koncentracija se izjednačava usled difuzionih pojava. U prisustvu membrane takođe dolazi do izjednačavanja koncentracije i to tako što rastvarač (voda) migrira iz manje ka većoj koncentraciji suve materije. Što je veća razlika u koncentraciji, to je veća i pogonska sila koja tera molekule rastvarača da prolaze kroz membranu. U slučaju potrebe da se spreči izjednačavanje koncentracije, bilo bi potrebno da se primeni određeni pritisak u koncentrovanijoj sredini, koji bi se suprostavio ulasku molekula rastvarača i taj pritisak poznat pod nazivom osmotski pritisak a izjednačavanje koncentracija preko polupropustljive membrane naziva se osmoza.
Očigledno je da se osmotski pritisak povećava sa smanjenjem koncentracije vode. Istovremeno se menjaju i neke druge karakteristike: povećava se tačka ključanja, smanjuje se tačka zamrzavanja, smanjuje se ravnotežna relativna vlažnost, smanjuje se aktivnost vode itd.
Brojčana vrednost osmotskog pritiska direktno je proporcionalna koncentraciji i apsolutnoj temperaturi. Ova vrednost, za razblažene rastvore i to samo za neelektrolite, može se izračunati iz jednačine:
u = 103 c RT
gde su:
u – osmotski pritisak N/m2 (Pa),
c – koncentracija (mol/dm3),
R – 8,314 J/(mol °K).
Ako se radi o elektrolitima koji se usled disocijacije ˝raspadaju˝ na dva ili više jona, vrednost osmotskog pritiska se koriguje Van΄t Hoffovim izotoničnim koeficijentom ˝i˝.
Voda je jedan od važnih uslova za razmnožavanje mikroorganizama i njihovu destruktivnu aktivnost. Znajući efekat osmoze i potrebe mikroorganizama za vodom, možemo na određeni način da menjamo supstrat (namirnicu) čineći je nepodesnom za mikrobiološku aktivnost. Naime ako posmatramo ćelije mikroorganizama u kojima se nalazi voda sa rastvorenim supstancama, proizilazi da i u njima, usled neke koncentracije rastvorljivih materija, vlada određeni osmotski pritisak. U ćeliji većine mikroorganizama vlada osmotski pritisak od 0,3 do 0,6 MPa. Ako u okolnoj sredini (namirnici) povećamo koncentraciju suve materije, tako da ona bude veća u poređenju sa koncentracijom u ćeliji mikroorganizama, doći će do gubitka vode, odnosno do plazmolize ćelije mikroorganizama. Sa povećanjem koncentracije suve materije raste i osmotski pritisak; na principu osmoze, voda iz ćelije mikroorganizama (ćelijska opna = polupropustljiva membrana) prelazi u predeo veće koncentracije suve materije što dovodi do ˝isušivanja˝ mikroorganizama.
U određenom momentu ćelija će u tolikoj meri da ostane bez vode da će se narušiti normalni životni procesi, prestaće razmnožavanje – čime je prestalo i mikrobiološko kvarenje namirnica. Manje otporni mikroorganizmi će uginuti a određen broj mikroorganizama sačuvaće mogućnost reprodukcije određeno vreme, i ako se u tom vremenu stvore potrebni uslovi (ako se vrati voda), nastaviće sa normalnim životnim aktivnostima. Ovo znači da je moguće konzervisati bilo koju namirnicu primenom dovoljno visokog osmotskog pritiska.
Prema povišenom osmotskom pritisku najotpornije su plesni i osmotolerantni odnosno osmofilni kvasci – što znači da ovi oblici mogu da se adaptiraju i da se razmnožavaju i u relativno suvoj sredini (gde je velika koncentracija suve materije, odnosno visok osmotski pritisak).
.
Odnos mikroorganizma prema vodi
Voda u ćeliji biljnog i životinjskog tkiva ili u ćeliji mikroorganizama razlikuje se od ˝čiste˝ vode. Razlika je u raspodeli i koncentraciji jona (mineralnih materija) i drugih rastvorljivih supstanci u vodi u samoj ćeliji u poređenju sa vodom izvan ćelije.
Ova razlika se objašnjava polupropustljivošću ćelijske membrane, odnosno apsolutnom nepropustljivošću membrane za neke supstance.
Opšte je prihvaćeno da se voda u namirnici nalazi u dva oblika i to u slobodnom i u ˝vezanom˝ stanju. Za mikrobiološku aktivnost značajna je samo količina slobodne vode. Slobodnom vodom se naziva deo ukupne vode koja se ponaša kao rastvarač. Napon vodene pare ove vode skoro je jednak naponu ˝čiste˝ vode. Aktivnost ove vode je praktično jednaka nuli.
Vezana voda je preko fizičko-hemijskih veza uključena u komponente koje sačinjavaju suvu materiju ili su molekuli vode vezani međusobno, tako da nema mogućnosti da se ponaša kao rastvarač.
Voda je u biološkom sistemu mnogo čvršće vezana i to prvenstveno za proteine ćelija usled električnog polja polarizovanog molekula vode (-COO- i NH3- ).
Vezani deo vode poroznih i kapilarnih tela, kakva su namirnice, s obzirom na način vezivanja, može se svrstati u 4 forme i to:
a) hemijski vezana voda (kristalna voda) – zbog svoje polarnosti, molekuli vode preko hidroksilnih grupa vezani su jonskim vezamasa komponentama suve materije. Može se smatrati da ova voda ulazi u hemijski sastav namirnice i ne može da se odstrani bez narušavanja hemijske prirode jedinjenja;
b) adsorpciono vezana voda je u stvari polimolekulski sloj vode na površini pora i kapilara namirnica i uslovljava veoma malu vlažnost materijala;
Kad se govori o ˝vezanoj˝ vodi uopšte, najčešće se misli na adsorpciono vezanu vodu za koloide. Ona čini 1/10 ukupne količine vode i kako samo ime kaže, ulazi u sastav solvatacionog sloja hidrofilnih koloida (belančevine, skrob, pektin…).
S obzirom na prirodu veze, jasno je da je ovaj deo vode vezan slabijim silama u poređenju hemijski vezanom vodom.
c) kapilarno vezana voda je polimolekulski sloj vode u obliku vodene pare koja je adsorbovana na zidovima pora i kapilara. Utvrđeno je da je kapilarno vezana voda vezana za suvu materiju kako fizičkim (adsorpcija) tako i hemijskim vezama;
d) osmotski vezana voda ima poseban značaj kada se radi o namirnicama koje poseduju tkivo, odnosno ćelije. Kada je koncentracija u ćeliji veća od koncentracije izvan nje, voda iz okolne sredine difundira u unutrašnjost; znači da je osmotski vezana i omogućuje pojavu osmotskog pritiska.
Koji će deo od ukupne vode u namirnici da bude u vezanom stanju, u velikoj meri je uslovljeno hemijskim sastavom suve materije. Svako jedinjenje nema podjednaku mogućnost da veže vodu. Najviše vode vezuju proteini i to 0,15 – 0,35 g vode po jednom gramu proteina.
U zavisnosti od prirode namirnice potrebno je da namirnica sadrži određenu količinu vode ispod koje mikroorganizmi neće biti u stanju da je pokvare.
Različita granična vrednost vode neophodne za mikrobiološku stabilnost različitih namirnica može jedino da se objasni upravo različitim hemijskim sastavom, a time i različitom količinom slobodne vode.
U prethodnom tekstu je navedeno da se jedino slobodna voda ponaša kao rastvarač a sada se vidi da samo nju mogu da koriste mikroorganizmi, i zbog toga se slobodna voda često naziva i biološki aktivna voda.
.
Pojam aktivnosti vode
Živi organizmi koje danas poznajemo u potpunosti zavise od prisutnosti određene količine vode u tečnom stanju. Voda je osnovni rastvarač i neophodna je za sve reakcije u živom svijetu, pa zbog toga udeo vode izrazito utiče na rast i razmnožavanje mikroorganizama.
Reakcije u citoplazmi takođe se odvijaju u vodenom medijumu. Citoplazma je okružena membranom koja je propustljiva za molekule vode koji mogu slobodno prolaziti iz citoplazme u okolinu i obrnuto.
Da bi se odvijao aktivan rast mikroorganizama, citoplazma mora biti u tečnom stanju (ona je važna, za rast i preživljavanje, jer mnogi mikroorganizmi mogu preživeti, ali ne i rasti kada bi njihova citoplazma bila potpuno osušena). Voda u okolini živih organizama mora biti prisutna, ne samo u tečnom stanju kao čista voda ili rastvor, nego i kao voda u atmosferi u gasovitom stanju, ili kao vezana voda što se opisuje kao čvrsto stanje.
Koristan parametar koji nam pomaže u razumevanju pokretanja molekula vode iz okoline u citoplazmu i obrnuto, jest aktivitet vode, aw-vrednost. To je pokazatelj one količine vode kojom mikroorganizam zaista raspolaže u reakcijama metabolizma.
Aktivnost vode supstrata najprikladnije je definisati na sledeći način:
aw = pw/pwo
gde je pw – pritisak vodene pare iznad namirnice, a pwo – pritisak pare čiste vode na istoj temperaturi.
Često, pogotovo kad se radi o osušenim namirnicama, umesto aktivnosti vode govori o tzv. ravnotežnoj relativnoj vlažnosti (RRV). Između ravnotežne relativne vlažnosti i aktivnosti vode postoji odnos:
aw = RRV / 100.
Po pravilu, namirnice sadrže određenu količinu slobodne vode. Zbog toga neposredno iznad njih (u izolovanom sistemu) vlada određeni pritisak vodene pare. Veličina pritiska vodene pare iznad bilo koje namirnice uvek je manja u poređenju sa pritiskom vodene pare iznad rastvarača. S druge strane, u vazduhu koji okružuje namirnicu, praktično uvek postoji određena količina vodene pare koja poseduje određeni pritisak.
Ako je napon vodene pare u namirnici veći od parcijalnog pritiska vodene pare u vazduhu – jedan deo vodene pare će se izdvojiti iz namirnice, što znači da će se namirnica više osušiti. U obrnutom slučaju, usled prisustva različitih supstanci u namirnici koje vezuju određenu količinu vode, doći će do povećanja vlažnosti namirnice – ako je parcijalni pritisak vodene pare u vazduhu veći od napona vodene pare neposredno iznad namirnice.
Relativna vlažnost vazduha je u direktnoj vezi sa parcijalnim pritiskom vodene pare u vazduhu. U slučaju kada je napon vodene pare u vazduhu i iznad namirnice brojno jednak, namirnica u jedinici vremena i primi i otpusti istu količinu vode – tako da se njena vlažnost ne menja. Takva relativna vlažnost vazduha koja uslovljava da se sadržaj vode u namirnici ne menja – naziva se ravnotežna relativna vlažnost. Sa ovog aspekta posmatrano, može da se razmišlja o relativnoj ravnotežnoj vlažnosti kao jednom od limitirajućih faktora za destruktivnu delatnost mikroorganizama.
Poslednjih godina, mnogi istraživači su postavljali razna pitanja vezana za puno značenje pojma aktivnosti vode. Pre svega, aktivnost vode je definisana samo za sisteme koji predstavljaju termodinamičku ravnotežu, pri čemu se pretpostavlja da je parcijalni pritisak pare iznad namirnice jednak parcijalnom pritisku vode unutar namirnice, i takođe je definisan za specifičnu temperaturu i ukupni pritisak. Pretpostavka o ravnoteži je validna samo za beskrajno razblažene sisteme.
Većina namirnica srednje vlažnosti kao i osušene namirnice obično su neravnotežni sistemi. Na primer, postojanje dve različite staze (kraka) između adsorpcionih i desorpcionih izotermi (ova pojava poznata je pod nazivom histerezis), pokazuje, prema Franks-u (1991), odsustvo ravnoteže.
Prehrambeni materijal može biti u stanju termodinamičke nestabilnosti (lažna stabilnost) i povremeno ovo nestabilno stanje traje duže od održivosti proizvoda (Wolf et al., 1985, van der Berg and Bruin, 1981).
Osim toga sadržaj vlage u namirnici koji je u ravnoteži sa stvarnom RRV može biti izložen promenama tokom perioda vlažnosti.
Takođe mnogi višekomponentni prehrambeni sistemi, sastavljeni od dve ili više faza (čvrsta, tečna, vodena i uljana), ne mogu predstavljati ravnotežu između pojedinih faza zbog ograničenja u zakonima kinetike.
Ove neravnotežne situacije mogu imati važne, negativne ili pozitivne, interakcije na hemijsku i mikrobiološku stabilnost. Mali porast sadržaja vode u osušenoj namirnici može dovesti do nestabilnosti aw vrednosti. Nasuprot tome, veoma usporena kristalizacija amorfnih šećera u osušenim namirnicama (to može značajno povećati aw vrednost) će održati proizvod u stanju lažne stabilnosti tokom normalnog perioda trajanja. Druga, negativna neravnotežna situacija javlja se kada distribucija vlage u suvim namirnicama nije homogena; namirnica se može stvrdnuti ili pokazati rast plesni na površini dok unutrašnjost pakovanja ostaje netaknut.
Tehnološkim procesima se smanjuje sadržaj vode, u cilju sprečavanja razvoja mikroorganizama, ali tako da namirnice zadrže svoja senzorna svojstva. To se može uraditi na dva načina:
1. dodatkom soli, šećera ili aditiva smanjuje se aw jer se jedan dio vode veže za ove rastvorene supstance (hidratacija);
2. podvrgavanjem namirnice niskim temperaturama (hlađenje ili smrzavanje) smanjuje se temperatura i aw što usporava ili sprečava razvoj nekih mikroorganizama.
.
Sadržaj vode kao osnova rasta mikroorganizama u namirnicama
Jedan od najstarijih postupaka zaštite namirnica jeste sušenje. Zaštita namirnica sušenjem je direktna posledica uklanjanja ili vezivanja vode, bez koje mikroorganizmi ne bi mogli rasti ni razmnožavati se.
Optimalna aw za rast većine mikroorganizama je u opsegu od 0,99 – 0,98. Svaki mikroorganizam ima graničnu aw vrednost ispod koje neće rasti, formirati spore, ili proizvoditi toksične metabolite ( Beuchat, 1987 ). S obzirom na aw koja je u vezi sa mikrobiološkom stabilnosti, minimalne aw vrednosti koje omogućavaju rast različitih tipova mikroorganizama su velika briga.
Tabela 1. prikazuje aw vrednosti različitih namirnica i uzročnike njihovog mikrobiološkog kvara, pokazujući takođe podelu mikroorganizama na osmofilne i osmotolerantne.
Opsežne tabele sa minimalnim aw vrednostima za rast i proizvodnju toksina nekoliko patogenih i mikroorganizama koji izazivaju kvarenje su objavljene od strane mnogih autora (Corry, 1973; Beuchat, 1983, 1987; Gould, 1989).
Tabela 2 prikazuje minimalne aw-vrednosti za rast navedenih mikroorganizama pri njihovim optimalnim vrednostima pH, temperature i hranljivim vrednostima.
Nekoliko saznanja dobijenih iz literaturnih podataka i tabele 2 mogu se sumirati na sledeći način:
- granična aw-vrednost za rast, različita je za različite vrste mikroorganizama. Uopšteno, uobičajene bakterije koje izazivaju kvarenje su inhibirane na aw vrednosti oko 0,97; patogene klostridije na aw 0,94; većina bakterija iz roda Bacillus na aw vrednosti 0,93. Staphylococcus aureus je najotporniji patogeni mikroorganizam, može rasti u aerobnim na aw= 0,86 i anaerobnim uslovima na aw=0,91. Veliki broj kvasaca i plesni se mogu razmnožavati na aw ispod 0,86, dok neki osmofilni kvasci i kserofilne plesni imaju sposobnost rasta na aw vrednosti nešto iznad 0,6. Da bi se namirnica zaštitila snižavanjem aw vrednosti, aw vrednost bi trebali, najmanje, sniziti do 0,6. Potpuno dehidrirane namirnice, na primer, imaju aw oko 0,3 da bi mogle obuzdati ne samo mikrobiološki rast nego i druge fizičko-hemijske i biohemijske reakcije štetne za boju, teksturu, ukus i hranljivu vrednost namirnica.
- minimalna aw vrednost za rast je uvek jednaka ili manja od aw vrednosti za produkciju toksina.
- minimalna aw vrednost za rast zavisi od rastvora korišćenog za regulisanje aw. Gould (1989) je ustanovio da u nekim primerima uticaji rastvora mogu zavisiti od sposobnosti rastvora da prožima ćelijsku membranu, kao u slučaju glicerola, koji lako prožima membranu mnogih bakterija i zbog toga ima nižu inhibitornu aktivnost vode.
Tabela 1. Aktivnost vode i mikrobiološko kvarenje namirnica
| Područje aw ispod kojeg je inhibirana aktivnost mikroorganizama | Vrsta mikroorganizama | Neke namirnice sa tom aw |
| 1,00 – 0,95 | Gram-negativni štapićasti oblici bakterija, spore bakterija, neki kvasci | Namirnice koje sadrže do 40% šećera ili do 7% NaCl, mnoge vrste kobasica, sredina hleba |
| 0,95 – 0,91 | Najčešće okruglasti oblici bakterija, laktobacili, vegetativne ćelije | Namirnice sa oko 65% šećera ili sa 15% NaCl; neke vrste salama, trajni sirevi |
| 0,91 – 0,87 | Najveći broj sojeva kvasaca | Namirnice sa oko 55% šećera ili sa 12% NaCl; suva šunka, polutrajni sirevi |
| 0,87 – 0,80 | Najveći broj plesni; Staphylococus aureus | Brašno, pirinač, seme leguminoza sa sadržajem 15*-17% vlage; voćni kolači, kondenzovano zaslađeno mleko |
| 0,80 – 0,75 | Najveći broj halofilnih bakterija | Namirnice sa 26% soli, marcipan (sa 16-17% vode), đem, marmelada, voćni sirup |
| 0,75 – 0,65 | Kserofilne plesni | Zdrobljeno i delimično obrano zrno zobi (sa oko 10% vlage) |
| 0,65 – 0,60 | Osmofilni kvasci | Suvo voće sa 15-20% vode; karamelna masa sa oko 8% vode |
| 0,50 | Područje koje inhibira razvoj bilo kojih vrsta mikroorganizama | Testenine i začini sa 10-20% vode |
| 0,40 | Jaja u prahu sa 5% vode | |
| 0,30 | Biskvit, prepržen hleb, kora hleba – sadržaj vode oko 3-5% | |
| 0,20 | Mleko u prahu (2-3% vode), sušeno povrće (oko 5% vode), kukuruzne pahuljice) oko 5% vode) |
Tabela 2. Minimalna aktivnost vode neophodna za razvoj mikroorganizama izazivača kvara namirnica pri optimalnim vrednostima pH i temperature
| Mikroorganizam | aw |
| Zarazni patogeni | |
| Campylobacter jejuni | 0,99 |
| Aeromonas hydrophila | 0,97 |
| Shigella spp. | 0,96 |
| Salmonella spp. | 0,94 |
| Yersinia enterocolitica | 0,95 |
| Escherichia coli | 0,93-0,95 |
| Listeria monocytogenes | 0,90-0,92 |
| Vibrio parahaemolyticus | 0,94 (glicerol), 0,95 (NaCl), 0,96 (skrob) |
| Toksigeni patogeni koji stvaraju spore | |
| Clostridium perfringens | 0,93 – 0,95 |
| Clostridium botulinum A i proteolitički B rodovi | 0,94 |
| Clostridium botulinum E i neproteolitički rodovi B i F | 0,96 |
| Clostridium botulinum G | |
| Bacillus cereus | 0,96, 0,90 (glicerol), 0,96 (NaCl) |
| Toksigeni patogeni | |
| Staphylococcus aureus (anaerobni) | 0,91 |
| Staphylococcus aureus (aerobni) | 0,86 |
| Staphylococcus aureus (aerobni) | 0,93 (ksilitol) |
| Staphylococcus aureus (aerobni) | 0,95 |
| Staphylococcus aureus (aerobni) | 0,89 (glicerol) |
| Plesni i kvasci | |
| Aspergillus flavus | 0,80 |
| Aspergillus parasiticus | 0,82 |
| Botrytis cinerea | 0,90 |
| Byssoclamys nivea | 0,84 |
| Aspergillus ochraceus | 0,77 |
| Penicillium citrinum | 0,80 |
| Penicillium cyclopium | 0,81 |
| Eurotium spp. | 0,81 |
| Monascus bisporus | 0,66-0,73 |
| Saccharomyces cerevisiae | 0,61, 0,89 (glukoza), 0,90 (skrob), 0,92 (NaCl), 0,70 |
| Zygosacharomyces bisporus | 0,65 |
| Zygosacharomyces rouxii | |
| Torulopsis candida |
Većina svežih namirnica ima aw vrednost ispod 0,99. Objavljene minimalne vrednosti za rast odabranih mikroorganizama u namirnicama prikazane su u tabelama 3 i 4. Uopšteno, bakterije zahtevaju više aw-vrednosti nego gljive, a gram-negativne bakterije imaju više zahteve od gram-pozitivnih. Većina bakterija koje izazivaju kvarenje ne rastu ispod aw-vrednosti ispod 0,91, dok plesni uzročnici kvarenja rastu i pri vrednostima manjim od 0,80.
Od bakterija koje uzrokuju trovanja hranom, za Staphilococcus aureus je dokazano da raste i pri aw-vrednostima manjim od 0,86, dok Clostridium botulinum ne raste ispod 0,94.
Jedino kvasci i plesni rastu unutar šireg raspona aw-vrednosti u odnosu na bakterije. Najniža objavljena aw-vrednost za bakterije bilo kog tipa je 0,75 za halofilne bakterije, dok kserofilne plesni i osmofilni kvasci rastu pri aw-vrednostima od 0,65, odnosno 0,61.
Tabela 3. Minimalne aw-vrednosti pri kojima mikroorganizmi aktivno rastu
| Grupa mikroorganizama | aw,min |
| Većina bakterija izazivača kvara namirnica | 0.91 |
| Većina kvasaca izazivača kvara namirnica | 0.88 |
| Većina plesni izazivača kvara namirnica | 0.80 |
| Halofilne bakterije | 0.75 |
| Kserofilne plesni | 0.65-0.75 |
| Osmofilni kvasci | 0.60 |
Između aw temperature i hranljivih materija postoje određeni odnosi. Prvo pri bili kojoj temperaturi smanjuje se sposobnost rasta ako se aw -vrednost smanjuje. Raspon aw unutar koga se pojavljuje rast viši je pri optimalnoj temperaturi rasta; treće, prisustvo hranljivih materija povisuje raspon aw preko kojeg organizam može preživeti. Stoga, specifične vrednosti date u tabeli 3 treba uzeti samo kao referentne tačke, jer promene li se temperatura i sadržaj hranljivih materija, rast se može odvijati pri malim aw- vrednostima.
Rast mikroorganizama na različitim površinama veliki je problem u tropskim državama kada je relativna vlažnost vazduha velika, pa je atmosferska voda tada osnov mikrobiološkog rasta. U takvim uslovima uslovima mikroorganizmi rastu na tkaninama, šatorima i ostalim površinama na kojima se ni u tim područjima uz nisku relativnu vlažnost normalno ne pojavljuju. Najbolja metabolička aktivnost, najvećeg broja mikroorganizama, odvija se pri aw-vrednostima između 0,80 i 0,90 (tabela 3).
Gljive, najčešće, mogu rasti pri nižim aw-vrednostima nego ostali mikroorganizmi. Zbog toga gljive rastu na mnogim površinama na kojima raspoloživa voda ne može biti osnova za rast bakterija. Zato na hlebu rastu plesni a ne bakterije. Mikroorganizmi ne mogu rasti na niskim aw-vrednostima, pa se ta činjenica primenjuje u zaštiti mnogih proizvoda.
Tabela 4. Minimalne aw-vrednosti za rast gljiva koje uzrokuju kvarenje namirnica
| Organizam | Minimum aw |
| Candida utilis | 0,94 |
| Botrytis cinerea | 0,93 |
| Rhizopus nigricans | 0,93 |
| Mucor spinosus | 0,93 |
| Candida scottii | 0,92 |
| Trichosporon pullulans | 0,91 |
| Candida zeylanoides | 0,90 |
| Endomyces vernalis | 0,89 |
| Alternaria citri | 0,84 |
| Aspergillus glaucus | 0,70 |
| Aspergillus echinulatus | 0,64 |
Granična vrednost aktivnosti vode zavisi od vrste mikroorganizama, pH vrednosti (u kiseloj sredini granična vrednost je veća), parcijalnog pritiska kiseonika, prisustva hranljivih materija i dr. Smanjenjem aktivnosti vode u okolini, smanjuje se rast mnogih vrsta mikroorganizma. Ispod određene aktivnosti vode vegetativni oblici mikroorganizama postepeno izumiru. Na prestanak aktivnosti i brzinu odumiranja, pored aktivnosti vode utiču i brojni drugi faktori. Raspon aktivnosti vode koji je neophodan za rast utiče i na ostala fizičko-hemijska i prehrambena stanja.
Primenom postupaka konzervisanja namirnica baziranih na principu smanjenja aktivnosti vode, uopšteno može da se kaže da se ne postiže sterilnost takvih namirnica. Najčešće se radi o smanjenju broja mikroorganizama i njihovoj ireverzibilnoj aktivnosti.
U namirnicama sa smišljeno smanjenom aktivnošću vode (koncentrisan proizvodi: kondenzovano mleko, voćni koncentrati, sirupi, slatka, džemovi, marmelade; usoljeni proizvodi od mesa i neki proizvodi od povrća, osušene namirnice), pogotovu ako su u, čvrstom agregatnom stanju, na mikrobiološku aktivnost utiče kako aktivnost vode tako i temperatura skladištenja.
Temperatura, pogotovu u prvoj fazi skladištenja, utiče na primarnu mikrofloru i na promenu aktivnosti vode, čime indirektno utiče na mogućnost razvoja mikroorganizama. Pri znatnim kolebanjima temperature skladištenja dolazi do premeštanja (migracije) vode u okviru namirnice. Kao rezultat ove pojave nastaju određena mesta na proizvodu sa povećanim sadržajem vlage (povećana aktivnost vode), dok neka druga mesta postaju suvlja. Ovakve pojave mogu da vode do značajnih promena u brzini porasta i selekciji određenih tipova mikroorganizama. Prisutna mikroflora, usled sopstvenog sadržaja vode, lokalno povećava aktivnost vode – što omogućuje aktivnost mikroorganizama koji dotle nisu bili aktivni.
Iz svega ovoga se može zaključiti da namirnice sa aktivnošću vode 0,60 ili manjom mogu da se smatraju mikrobiološki stabilnim i to je tzv. granična vrednost za mikrobiološki rast. To znači da se ova vrednost aktivnosti vode može smatrati kritičnom; svako povećanje preko ove vrednosti daje mogućnost razvoja nekih vrsta mikroorganizama, odnosno može da dovede do mikrobiološkog kvarenja takve namirnice. Maksimalan sadržaj ukupne vode koji garantuje mikrobiološku stabilnost, ali ne mora da uslovljava aw= 0,60, za neke namirnice je sledeći:
- mleko u prahu 8%,
- jaja u prahu 10-11%,
- brašno 13 -15%,
- pirinač 13 – 15%,
- suvo meso 15%,
- suvo voće 20 – 25%,
- suvo povrće 5 – 10%.
Iako količina vode (odnosno koncentracija suve materije) ne daje tačan podatak o aktivnosti vode, jer relativno male promene u suvoj materiji (hidroliza saharoze, skroba i dr.) u velikoj meri utiču na kapacitet vezane vode; tj. pri istoj sadržini vode menja se aktivnost vode, postoji određena korelacija između količine vode nekih namirnica i aktivnosti vode.
Iz ovih razmatranja proizlazi da ako nije postignuta potrebna vrednost suve materije (aktivnosti vode) za onemogućavanje mikrobiološke aktivnosti, moraju dodatno da se koriste toplota, hemijski konzervansi, inertni gas, posebni uslovi skladištenja ili neki drugi zahvati kojima se neće dozvoliti razvoj mikroorganizama.
.
Kombinovanje kontrole aktivnosti vode sa drugim tehnikama konzervisanja
Najvažnija tehnike, koje se obično koriste u cilju zaštite prehrambenih proizvoda, više deluju tako što inhibiraju rast mikroorganizama nego inaktivirajući ih (Gould, 1995). Među inhibitorne tehnike spadaju :
- smanjenje aktivnosti vode (konzevisanje, sušenje, isparavanje)
- temperatura (visoka ili niska)
- kiselost ili smanjenje pH dodavanjem neorganskih i organskih kiselina
- redoks potencijal (Eh), konzervansi (npr., nitriti, sorbati, sulfiti)
- konkurentni mikroorganizmi (npr.,bakterija mlečne kiseline)
- pakovanje u modifikovanoj atmosferi (vakuum, vodonik, ugljen- dioksid, kiseonik).
S druge strane, nekoliko tehnika deluju tako što inaktiviraju mikroorganizme u hrani. Toplota je daleko najkorištenija tehnika inaktiviranja ( pasterizacija, sterilizacija), sa sve većom upotrebom alternativnih rešenja kao što su jonizujuće zračenje kao i nove, ‘razvijene’ tehnologije kao što su visok hidrostatički pritisak, ultrazvuk, ultraljubičasto svetlo i svetlosni impulsi visokog intenziteta (Gould, 2000; Leistner, 2000).
Kao što je navedeno prema Leistner-u(1978, 1987) skoro je postalo jasno da, u većini namirnica za koje je aw-vrednost značajan pokazatelj kvaliteta i stabilnosti, drugi faktori, koje on naziva ‘prepreke’, doprinose željenom kvalitetu proizvoda, pa početno interesovanje za aktivnost vode od strane proizvođača hrane, prošireno je i na te faktore (npr., Eh, pH, temperaturu, dodavanje aditiva, itd.). Cilj je bio postići stabilnost proizvoda a temelji se na razumnom kombinovanju faktora usled kombinovanja tehnologije konzervisanja ili tehnologije ‘prepreka’. Više od 60 potencijalnih ‘prepreka’ za namirnice životinjskog ili biljnog porekla, koja poboljšavaju stabilnost i / ili kvalitete ovih proizvoda, su već opisani, a popis mogućih ‘prepreka’ za konzervisanje hrane ni u kom slučaju nije kompletan (Leistner, 2000).
Prema Leistner-u u namirnicama konzervisanim tehnologijom ‘prepreka’ postoji mogućnost da različite ‘prepreke’ u namirnici neće imati samo uticaja na stabilnost , ali mogu delovati sinergstički. Sinergističko delovanje može se dobiti ako ‘prepreka’ u namirnici pogađa različite mete (npr. ćelijsku membranu, DNK, enzimske sisteme, pH, aw, Eh itd.) unutar ćelije mikroorganizama a time remeti homeostaze prisutnih mikroorganizama na nekoliko načina. Zbog toga korišćenje različitih ‘prepreka’, u cilju očuvanja određenih namirnica, bi trebalo imati prednosti zbog toga što se mikrobiološka stabilnost može postići kombinacijom nežnih ‘prepreka’.
U praksi to može značiti da se bolji rezultati postižu tako što se u namirnicu doda više različitih konzervanasa u manjim količinama nego samo jednog ali u većoj količini, jer različiti konzervansi mogu pogoditi različite mete unutar bakterijske ćelije a time deluju sinergistički.
Mikrobiološka stabilnost i senzorni kvalitet većine namirnica danas se zasnivaju na kombinaciji ‘prepreka’. Tehnologija ‘prepreka’ se dokazala korisnom u optimizaciji tradicionalnih namirnica isto tako dobro kao i u razvoju novih proizvoda. Kako bilo, aw-vrednost će biti jedna od glavnih prepreka kojom se može manipulisati a upotreba kombinacija spoljašnjih i unutrašnjih faktora zajedno sa sniženom aw-vrednosti su uobičajeni u prehrambenoj industriji.
Uglavnom, ako je minimalna vrednost aktivnosti vode za rast mikroorganizama postignuta, promene drugih okolnih faktora će imati veći uticaj na smrt ili opstanak istih.
.
Merenje i prognoza vrednosti aktivnosti vode u namirnicama
1. Merenje vrednosti aktivnosti vode
Brze, povoljne i pouzdane laboratorijsko-analitičke metode merenja aw-vrednosti su veoma tražene u prehrambenoj industriji i u istraživačkim laboratorijama za potvrdu kvaliteta i pri izboru uslova skladištenja namirnica. Ovo se posebno odnosi na namirnice u kojima je kontrola aw-vrednosti kritična pri određivanju mikrobiološke aktivnosti i bezbednosti.
Neki od instrumenata za određivanje aw-vrednosti koji se uglavnom koriste su:
a) Manometri za merenje pritiska vodene pare
Pri ovom postupku namirnica se stavlja pod vakuum što joj omogućava da uspostavi ravnotežu (na kontrolisanoj temperaturi) sa okolnim vazduhom tj. napon pare okolnog vazduha je u ravnoteži sa naponom pare ispitivanog uzorka. Pošto je potrebno dosta vremena da bi se postigla ravnoteža ova metoda nije pogodna za brze rutinske analize.
Metode zasnovane na ovom principu su uzete kao referentne sa kojima se porede druge metode i uređaji. Ova tehnika se ne može koristiti za rad sa živim i fermentisanim materijalima i zahteva osetljivost od 0,01 mmHg pri merenju pritiska. Tačnost ove metode je ±0,005 aw-jedinica pri vrednostima aktivnosti vode manjim od 0,85 ali pri većim vrednostima tačnost iznosi 0,02 jedinice zbog problema kondenzacije i kontrole temperature.
b) Higrometar za određivanje tačke rosišta (dostupni instrumenti: Decagon, EG&G, General Eastern)
Ova metoda se zasniva na kondenzaciji vodene pare na površini ogledala koje je hlađeno do temperature rose u atmosferi izazvanoj ispitivanjem uzorka. Tačka rose ustanovljena fotoelektrički i povezana je sa aw-vrednosti korištenjem psihrometarskih dijagrama. Ovaj uređaj se koristi da se utvrdi aw u širokom opsegu (tačnost: ±0,005 aw jedinica) i takođe omogućava merenje na različitim temperaturama. Merenje je veoma brzo (oko 2 min) ali može biti usporeno u slučaju kondenzacije na nižim kritičnim temperaturama nego što je za vodu i nečistoćom površine ogledala.
c) Metode sniženja tačke mržnjenja (dostupni instrumenti: Advanced Instrument Milk Crioscope)
Snižavanje tačke mržnjenja kao i promene u drugim koligativnim osobinama, mogu biti kvantitativno povezane sa aw-vrednostima (Robinson and Stokes, 1965). Ova metoda je pogodna za merenje aw vrednosti, uglavnom, tečnih namirnica sa aw >0,97 (preciznost: ±0,0004) iako se preporučuje i za vrednosti niže od 0,80 takođe za tečne ekstrakte ali i za homogene čvrste namirnice ( Ferro Fontan nd Chirife, 1981). Aw-vrednosti izračunate merenjem tačke mržnjenja ne razlikuju se mnogo od vrednosti izmerenih na 25°C (razlike su manje od 0,01 aw-jedinice).
d) Električni higrometri
Ovi instrumenti se baziraju na tri tipa senzora vlažnosti:
1. Senzori formirani od električne žice prevučene visoko-higroskopnom solju, obično litijum- hloridom (LiCl), čija električna provodljivost ili otpornost zavise od stepena hidratacije a samim tim i od relativne vlažnosti uzorka (u ravnoteži sa senzorom) (dostupni instrumenti su: Beckman, Novasina, Rotronic, American Instrument).
2. Senzori napravljeni od tečne higroskopne supstance koja absorbuje i desorbuje vlagu (prima i otpušta vlagu) i čija se el. impedanca menja sa sadržajem vlage.
3. Senzori sastavljeni od tankog polimernog nosioca čiji se kapacitet menja proporcionalno relativnoj vlažnosti (dostupni instrumenti: Vaisala, General Eastern, WeatherMeasure).
Za sva tri tipa sistema merenja interval pouzdanosti se kreće u opsegu od ±0,005 aw-jedinica.
Neki proizvođači obezbeđuju filtere u cilju zaštite senzora ali oni, kao što je poznato, produžuju vreme potrebno za uspostavljanje ravnoteže pre očitavanja aw vrednosti (Chirife, 1995).
Drugi zabeleženi problemi su potreba za učestalom kalibracijom i njihova zavisnost od temperature, netačnost na određenim vrednostima aktivnosti vode, starenje senzora i uticaj histerezisa na vioke aw
vrednosti. U svakom slučaju, rad ovih higrometara razlikuje se od ostalih komercijalnih instrumenata koji su dostupni.
e) Higrometar sa vlaknima (dostupni instrumenti: Abbeon, Lufft)
Ovaj instrument kao senzor koristi sintetičku, poliamidnu nit koja se skuplja kada je izložena visokoj relativnoj vlažnosti. Vreme uspostavljanja ravnoteže između namirnice i vlakna je približno 3 sata sa tačnošću od ±0,01 aw jedinice. Odziv senzora je na poseban način pogođen temperaturnim promenama i prisustvom isparljivosti. Ostali problemi koji se mogu javiti pri upotrebi ovog uređaja su histerezisi (petlje) kao i starenje senzora. Uprkos njegovoj niskoj osetljivosti kao i relativno niskoj ceni, higrometar sa vlaknima se dosta koristi za rutinska ispitivanja u prehrambenoj industriji.
Direktno merenje pritiska vodene pare je ekstremno teško a indirektne metode su obično korišćene za određivanje aw-vrednosti.
Tačnost dobijena korišćenjem indirektnih metoda zavisi od dobijanja kalibracione krive sa referentnim standardima u intervalu aw koji nas interesuje (Favetto et al, 1983).
Pet različitih izvora je predloženo kao zgodan broj tačaka za konstrukciju kalibracione krive.
Mora se naglasiti da se siromašni rezultati dobijaju kada su instrumenti kalibrisani prema proizvođačkim zahtevima.
Zasićeni rastvori soli preporučeni su od strane mnogih radnika kao pogodan, lagan i tačan način da se obezbede rastvori poznate aw-vrednosti. To su reproduktivni referentni standardi zato što merenje koncentracije nije potrebno i ako su soli pravilno izabrane ometajuće pare nisu prisutne. Kako god, većina izveštaja u literaturi se ne poklapa po pitanju aw vrednosti svakog od zasićenih rastvora soli (Greenspan, 1997; Labuza et al, 1976 ).
tabela 5. Aktivnost vode odabranih zasićenih rastvora soli koji se koriste kao standardi
| SO | 10 ° C | 15 ° C | 20 ° C | 25 ° C | 30 ° C |
| Litijum-bromid | 7,1 | 6,9 | 6,6 | 6,4 | 6,2 |
| Natrijum- hidroksid | 9,6 | 8,9 | 8,2 | 7,6 | – |
| Litijum- hlorid | 11,3 | 11,3 | 11,3 | 11,3 | 11,3 |
| Kalijum- acetat | 23,5 | 23,5 | 23,0 | 22,5 | 22,0 |
| Magnezijum- hlorid | 33,5 | 33,0 | 33,0 | 33,0 | 32,5 |
| Kalijum- karbonat | 44,0 | 43,5 | 43,0 | 43,0 | 43,0 |
| Natrijum-bromid | 60,0 | 59,0 | 58,0 | 57,7 * | 56,5 |
| Bakar- hlorid | 68,0 | 68,0 | 68,0 | 67,5 | 67,0 |
| Kalijum- jodid | 72,0 | 71,0 | 70,0 | 69,0 | 68,0 |
| Natrijum- hlorid | 76,0 | 75,5 | 75,5 | 75,3 * | 75,0 |
| Amonijum- sulfat | 81,0 | 80,5 | 80,5 | 80,1 * | 80,0 |
| Kalijum- hlorid | 87,0 | 86,0 | 85,0 | 84,3 * | 84,0 |
| Natrijum- benzoat | 88,0 | 88,0 | 88,0 | 88,0 | 88,0 |
| Barijum- hlorid | 91,0 | 90,6 | 90,2 * | 89,9 | – |
| Kalijum- nitrat | 95,5 | 95,0 | 94,0 | 92,5 * | 92,0 |
| Kalijum- sulfat | 98,0 | 98,0 | 97,5 | 97,2 * | 97,0 |
2. Prognoza vrednosti aktivnosti vode u praksi
Na aw se može uticati na najmanje 3 načina u toku pripreme namirnica sa niskim, srednjim i isokim sadržajem vlage:
1. Voda se može ukloniti dehidratacijom, isparavanjem ili koncentrisanjem.
2. Dodatkom odgovarajućeg rastvora. Impregnacija rastvora se može izvesti vlažnim ili suvim ulivanjem (infuzija). Vlažna infuzija se sastoji od natapanja komadića u vodenom rastvoru niže aw-vrednosti dok suva infuzija uključuje direktno mešanje komadića i rastvora u određenim odnosima.
Kad se čvrsti proizvodi bogati vodom, kao što su voće i povrće, podvrgnu vlažnoj ili suvoj infuziji odigravaju se tri toka :
– prelazak vode iz namirnice u okolinu;
– tok rastvorene supstance, iz okoline u proizvod, i
– izdvajanje rastvorenih supstanci iz samog proizvoda.
Ovaj proces se zove OSMOTSKA DEHIDRATACIJA i dopušta infuziju ne samo rastvora korišćenog za kontrolu aw, već i infuziju željenih količina antimikrobnih sredstava i sredstava protiv tamnjenja ili bilo kog rastvora za poboljšanje senzornog i nutritivnog kvaliteta hrane.
Kontrolišući ove složene promene moguće je razumeti različite kombinacije gubitka vode i priraštaja suve materije od najprostijeg procesa uklanjanja vode ( uklanjanje vode je na prvom mestu a primanje šećera samo u marginalnim delovima namirnice) pa do procesa kandiranja i soljenja (favorizovano je prodiranje rastvora a uklanjanje vode je ograničeno).
3. Kombinacija 1. i 2., kada su djelići namirnica infuzrani rastvorima i aditivima a zatim posebno sušeni.Prednosti koje se postižu ovom kombinacijom, koja je poređena sa samim sušenjem, su povećanje stabilnosti pigmenata odgovornih za boju, pojačanje prirodne arome, bolja tekstura itd.
Bez obzira koji postupak za redukciju aw vrednosti koristili, potrebno je poznavati vezu između aktivnosti vode i sadržaja vlage u namirnicama.
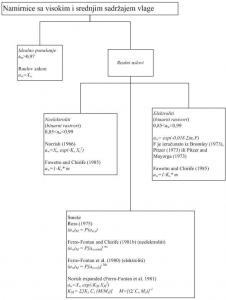
Xw: molarna frakcija vode; Xs: molarna frakcija rastvorka; Ks: Norrish-ova konstanta za neelektrolit s; Ks*: konstanta za svaki rastvorak (elektrolit ili neelektrolit); m: molalitet; mi =vm, gde je v broj jona po molu rastvorene supstance i; Φ: osmotski koeficijent; (aw)M : aktivnost vode složenih rastvora; (aw,s): aktivnost vode svake s komponente kada se merenje vrši pri istom molalitetu kao kod kompleksnog rastvora; ms: molalitet s komponente u smeši; ms(l): ukupni molalitet rastvorene supstance koja bi proizvodila jonsku silu jednako za svaku smešu; aw,s(l): aktivnost vode rastvorka s u binarnom rastvoru pri molalitetu ms(l); Cs: masa rastvorka s / masa ukupne čvrste supstance; Ms: molarna masa rastorka s.
Shema 1. Šema i izabrani modeli za praktično određivanje aktivnosti vode u vlažnim i delimično vlažnim namirnicama
Ne postoji model sa jednostavnom matematičkom strukturom koji je sposoban za predstavljanje sorpcije ili karakteristika snižavanja aw vrednosti u namirnicama ili njihovim komponentama u čitavom intervalu vodene aktivnosti, od kako je smanjenje aw vrenosti izazvano kombinovanjem svakog od mehanizama koji mogu biti predominantni za navedeni interval.
U namirnicama sa srednjim i visokim sadržajem vlage, aw je uglavnom određena samom prirodom namirnice i koncentracijom soljubilnih supstanci (šećera, NaCl, aminokiselina, organskih molekula i
drugih soli) u vodenoj fazi namirnice. Brojne jednačine, bazirane na termodinamičkim osobinama binarnih i višekomponentnih elektrolitičkih i neelektrolitičkih rastvora, su teoretki i eksperimentalno ispitivane u cilju računanja ili određivanja aw vrednosti ovih proizvoda.
Šema 1. sumira nekoliko teoretskih i empirijskih modela predloženih za računanje aw vrednosti u delimično i potpuno vlažnim namirnicama (van der Berg and Bruin, 1981; Chirife, 1995).
U namirnicama sa niskim sadržajem vlage, adsorpcija vode na površinu je odgoorna za redukciju aw vrednosti (Chirife and Iglesias, 1978).
Iako fizička hemija površinskih slojeva namirnica snadbeva naučnike iz oblasti prehrambene tehnologije sa velikim brojem toretskih jednačina, veza sorpcija vode – aw vrenost ne može biti predviđena ali može biti eksperimentalno određena iz mnogo razloga.
.
Literatura
1. Duraković S., Delaš F., Stilinović B., Duraković L.(2002): Moderna mikrobiologija namirnica, Kugler, Zagreb
2. Vereš M. (1991), Principi konzervisanja namirnica, Poljoprivredni fakultet, Beograd
3. Zeuthen P., Bogh-Sorensen L. (2003): Food preservation techniques, Cambridge Press, England