Autor: Zdravko Šumić
Mentor: prof. dr Spasenija Milanović
Proteini mlijeka sastoje se od kazeina, koji čini 80% svih proteina u mlijeku, i proteina mliječnog seruma (surutke) koji čine 20%. Pored njih se u neznatnim količinama nalaze još i enzimi i neki minorni proteini (Đorđević, 1987). Kazein se sastoji iz više frakcija (a, b, g), dok se serum proteini sastoje iz više albumina i globulina.
Mlijeko sadrži oko 3-3,5% (30-35 g/l) proteina što čini oko 28% suve materije. Ovo govori da je mlijeko namirnica bogata proteinima. Proteini se nalaze u mlijeku u obliku micele, globularnog oblika.
Tabela 3. Sastav proteina mlijeka
| protein | (%) |
| Kazein | 81 |
| a– kazein | 62 |
| as- kazein | 50 |
| k– kazein | 12 |
| b– kazein | 30 |
| g– kazein | 5 |
| Serum | 19 |
| laktoalbumini | |
| b– laktoglobulin | 10 |
| a– laktoalbumin | 4 |
| krvni serum albumin | 1 |
| laktoglobulini | |
| euglobulin | 1 |
| pseudoglobullin | 1 |
| imunoglobulin | 2 |
| frakcija proteoza i peptona | 4 |
Naziv kazein potiče od latinske riječi caseus što znači sir, jer je on supstanca čijim se zgrušavanjem omogućava proizvodnja sira i predstavlja osnovni protein u njemu. Kazein je najvažniji protein mlijeka ne samo zato što ga najviše ima već i zbog njegovih tehnoloških osobina. Mnoge tehnologije mlijeka zasnovane su na osnovnim osobinama kazeina (tehnologija sira, mliječno-kiselih proizvoda) ( Đorđević, 1987).
.
Elementarni sastav kazeina
Kazein sadrži nešto manje azota nego većina drugih proteina, što je posljedica aminokiselinskog sastava, prisustva P, šećera i njihovih derivata.
Sadržaj najzastupljenijih elemenata u proteinima mlijeka je sljedeći: C 52,5%, O 22,3%, N 15,6%, H 7,1%, P 0,8%, S 0,7%.
Navedeni sadržaj P u kazeinu odnosi se na organski P, koji predstavlja konstitucioni dio kazeinske micele (u obliku fosforne kiseline vezan za peptidne lance hemijskim vezama). Takozvani neorganski P je u vidu različitih soli adsorbovan na površini kazeinskih čestica i utiče u određenoj mjeri na njihovu stabilnost.
Sumpora u kazeinu ima relativno malo što govori o relativno maloj količini tioamino kiselina cisteina i metionina. Zbog nedostataka ovih esencijalnih aminokiselina biološka vrijednost kazeina je nešto niža. Međutim, proteini surutke sadrže više nego dvostruko veću količinu tioamino kiselina od kazeina pa imaju komplementarnu ulogu i čine da ukupna biološka vrijednost ukupnih proteina mlijeka bude znatno veća (Đorđević, 1987).
.
Aminokiselinski sastav kazeina
Kazein je potpun protein jer sadrži sve aminokiseline koje ulaze u sastav proteina. Treba praviti razliku između kompletnog proteina i njegove biološke vrijednosti, koja zavisi od odnosa i zastupljenosti pojedinih aminokiselina u njemu.
Kazein sadrži relativno velike količine glutaminske kiseline i prolina, pored toga sadrži i znatne količine leucina, lizina, valina i asparaginske kiseline (Đorđević, 1987).
.
Opšte osobine
Izdvojen iz mlijeka kazein predstavlja bijelu amorfnu supstancu koja je praktično rastvorljiva u vodi i nerastvorljiva u organskim rastvaračima. Kazein se može izdvojiti iz mlijeka isoljavanjem sa NaCl. Takođe, i CaCl2, CuSO4, FeSO4 kao i neke stipse (npr. ![]() ), ali u znatno manjim koncentracijama omogućavaju izdvajanje kazeina iz mlijeka. Ova osobina koristi se u analitičke svrhe.
), ali u znatno manjim koncentracijama omogućavaju izdvajanje kazeina iz mlijeka. Ova osobina koristi se u analitičke svrhe.
U prisustvu veće količine etanola dolazi do koagulacije kazeina, jer alkohol izaziva koagulaciju kazeinskih čestica, utiče na njihove elektro-hemijske osobine što dovodi do njihove koagulacije.
Koncentracija alkohola pri kojoj dolazi do koagulacije zavisi od niza faktora, a najvažniji su kiselost sredine i koncentracija ![]() . Ukoliko je kiselost sredine veća potrebna je manja koncentracija alkohola za zgrušnjavanje. To znači da ova dva faktora sadejstvuju u dehidrataciji, pa prema tome i u destabilizaciji kazeinskih čestica. Povećana kiselost izaziva izdvajanje dijela Ca iz Ca-kazeinatno fosfatnog kompleksa u jonizovani oblik što dovodi do povećanja destabilišućeg efekta. Povećana količina
. Ukoliko je kiselost sredine veća potrebna je manja koncentracija alkohola za zgrušnjavanje. To znači da ova dva faktora sadejstvuju u dehidrataciji, pa prema tome i u destabilizaciji kazeinskih čestica. Povećana kiselost izaziva izdvajanje dijela Ca iz Ca-kazeinatno fosfatnog kompleksa u jonizovani oblik što dovodi do povećanja destabilišućeg efekta. Povećana količina ![]() jona ima za posljedicu ukrupnjavanje kazeinskih čestica usljed čega su one manje stabilne, pa dodavanje alkohola u količini koja u normalnom mlijeku ne bi izazvala zgrušnjavanje, u ovim uslovima ga zgrušnjava (Carić, Milanović, 1997).
jona ima za posljedicu ukrupnjavanje kazeinskih čestica usljed čega su one manje stabilne, pa dodavanje alkohola u količini koja u normalnom mlijeku ne bi izazvala zgrušnjavanje, u ovim uslovima ga zgrušnjava (Carić, Milanović, 1997).
Ove pojave čine osnovu tzv. alkoholne i alizarolne probe, koje se primjenjuju kao rutinske, brze metode pri prijemu mlijeka u mljekaru. Njima se, dakle, utvrđuju uzorci mlijeka sa povećanom kiselošću ili drugim prirodnim poremećajima.
.
Elektroforetske osobine kazeina
Primjenom elektro-hemijskih metoda analize otkrilo se da kazein izdvojen iz mlijeka ne predstavlja jedinstvenu homogenu supstancu. Primjenom metode gel elektroforeze i elektroforeze pokretne granice došlo se do toga da se kazein sastoji iz tri oblika (frakcije) a, b i g.
a -kazeinom je nazvana komponenta kazeina koja najdalje migrira od mjesta nanošenja uzorka (tj. ona koja ima najveću migracionu brzinu), dok je g -kazein komponenta koja je najmanje odmakla od mjesta nanošenja uzorka (Carić, Milanović, 1997).
.
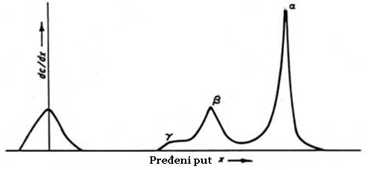
Elektroforetogram kazeina
Na slici 1 se može uočiti pređeni put a, b i g kazeina. Površine koje zahvataju pojedina krive (pikovi) su proporcionalne sadržaju pojedinih elektroforetskih komponenata u kazeinu. Prosječna zastupljenost ovih komponenata u ukupnom kazeinu iznosi a : b : g = 66 : 19 : 5. Postoje značajna odstupanja od ovih prosječnih vrijednosti. Na njihov odnos utiče više faktora, a najznačajnija su rasa krava i period laktacije (Đorđević, 1987).
Slika 1. Elektroforetogram kazeina
Pojedine komponente kazeina razlikuju se i po elementarnom sastavu. Tako je a najbogatiji u azotu i fosforu, a najsiromašniji u sadržaju sumpora od svih komponenata. Kod g je situacija obrnuta; najsiromašniji je od svih komponenata po sadržaju azota i fosfora, a najbogatiji u sadržaju sumpora.
Usavršavanjem elektroforetskih metoda otkrilo se da a nije homogen i razdvojen je na dvije glavne komponente: as i k. Kasnije je utvrđeno da je i as elektroforetski heterogen (as0, as1 i dr.). Slovo s u indeksu as, označava da je ova komponenta osjetljiva na ![]() (s – sensitive, osjetljiv), tj. koaguliše.
(s – sensitive, osjetljiv), tj. koaguliše.
k – kazein ima ulogu zaštitnog koloida i njegovo prisustvo spriječava koagulaciju kazeina u mlijeku koje je presićeno kalcijumom. Ovo svojstvo on ima zahvaljujući svom hidrofilnom dijelu koji u sebi sadrži različite šećere (glukoza, galaktoza, manoza i dr.). Pod dejstvom himozina (sirišni enzim) dolazi do odvajanja ovog dijela pa ukupni kazein postaje osjetljiv na dejstvo ![]() jer se gubi zaštitna uloga k – kazeina.
jer se gubi zaštitna uloga k – kazeina.
Elektroforetskim ispitivanjima je ustanovljeno da se pri razdvajanju pojedinih komponenata kazeina, u različitim uzorcima mlijeka, za iste komponente dobijaju različite Rm vrijednosti (relativna mobilnost). Do ovoga dolazi usljed razlike u broju i vrstama pa prema tome i u redoslijedu aminokiselina u peptidnom lancu. Ove varijacije uslovljene su genetskim faktorima tj. nasljedne su. Genetski polimorfizam pokazuju as, b i g -kazein. Postoje četiri genetske varijante označene slovima A, B, C i D pri čemu najveću Rm vrijednost ima A, a najmanju C.
Ove varijante nisu podjednako zastupljene kod različitih rasa, čak ni u okviru jedne rase. Najmanje genetskih varijanti ima kod onih rasa koje su genetski stabilizovane, a više ih ima kod onih rasa koje su nastale ukrštanjem. Pojava ovih varijacija naziva se polimorfizam kazeina.
U mlijeku postoji kazein u obliku micela (cijeli kazein) a ne a, b, g i drugi kazeini. Kada se razmatraju tehnološke osobine mlijeka govori se o kazeinu, o njegovom ponašanju, a ne o ponašanju a, b, g i drugih kazeina, jer osobine ovih elektroforetskih komponenata su toliko različite od osobina i ponašanja kazeina da se najčešće ne mogu ni porediti. Dakle, ove elektroforetske komponente su sastojci međusobno povezane u jedinstveni protein – kazein.
Utvrđeno je da g kazein predstavlja u stvari dio peptidnog lanca b kazeina tako da se danas g- kazein izostavlja kao kazein. Iz ovoga proizilazi da i ostali elektroforetski kazeini predstavljaju esencijalne dijelove kazeina, bez obzira da li su u njemu zastupljeni u vidu cijelih peptidnih lanaca ili predstavljaju njihove razdvojene dijelove.
.
Struktura kazeina
Kod kazeina razlikuje se primarna, sekundarna, tercijarna i kvaternerna struktura.
Primarnu strukturu karakteriše broj i redoslijed aminokiselina u peptidnim lancima kao i mjesto i način vezivanja ostalih komponenata (fosforna kiselina, šećeri, derivati šećera) na aminokiselinskom nizu. Molekul kazeina (osnovna kazeinska micela) je veoma složen i do danas nije poznat tačan broj peptidnih lanaca, njihova veličina, niti sigurno način na koji su povezani u osnovnoj miceli kazeina (Đorđević, 1987).
Pod sekundarnom strukturom podrazumjeva se oblik lanca u sastavu proteina. U suštini razlikuju se dvije varijacije: longitudinalna i spiralna. Prvi je dakle, izduženi oblik, dok spiralni oblik nastaje kao posljedica međusobnog dejstva reaktivnih grupa lanca usljed čega dolazi do obrazovanja zavojnice. Smatra se da polipeptidni lanci u miceli kazeina imaju uglavnom longitudinalni oblik.
Tercijarna struktura predstavlja vid uklapanja (pakovanja) u globularnu formu. Lanci se međusobno povezuju preko disulfidnih veza, fosfatne veze preko Ca, vodoničnih veza, Londonovih i Van der Valsovih sila. Kazein je globularni protein.
Kvaterna struktura nastaje kao rezultat asocijacije monomera (molekula) kazeina usljed čega se obrazuju krupni asocijati tj. krupnije micele. Obrazovanje asocijata kod kazeina je veoma izraženo – kazeinske čestice. Kazein ima homogenu kvaternernu strukturu s obzirom da ne postoje razlike u sastavu između asocijata različitog stepena polimerizacije. Veličina asocijata zavisi od koncentracije proteina, pH, temperature. Osobina je ovih asocijata da se stvaraju pod određenim, ali i da se disociraju na sastavne dijelove, pod drugim uslovima sredine (Đorđević, 1987).
.
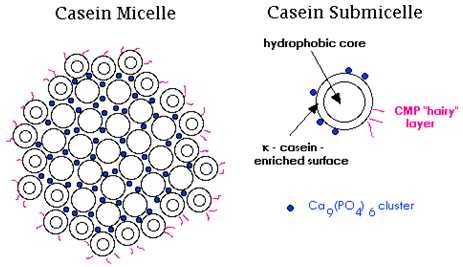
Struktura kazeinske micele
U mlijeku se kazein nalazi u obliku kompleksnih micela (slika 2), koje se često nazivaju i kazeinskim česticama. Ta kompleksnost proističe iz dva razloga:
- pored složenog proteinskog dijela kazein sadrži i Ca, Mg u obliku fosfata i citrata. Pored toga Ca se nalazi djelimično vezan direktno za protein dok se drugim dijelom nalazi u obliku soli fosforne kiseline.
- kazeinske micele imaju sposobnost da se agregiraju ili dezagregiraju u zavisnosti od uslova sredine. Dakle, mogu da se povećavaju ili smanjuju što uključuje i pitanje kvaterne strukture.
Najmanja prirodna kazeinska micela koja ima sve osobine cijelog kazeina naziva se monomerom. Umnožavanjem broja monomera u jednoj čestici većih dimenzija dobijaju se polimeri (Đorđević, 1987).
Slika 2. Struktura kazeinske micele
U mlijeku se kazein nalazi u obliku monomera i polimjera. Monomeri predstavljaju mali dio cijelog kazeina u mlijeku (3 – 10%). To je onaj dio kazeina koji se ne izdvaja prilikom ultracentrifugisanja već ostaje dispergovan u tečnosti i naziva se rastvorljivi kazein ili kazein mliječnog seruma. Odnos monomernog i polimjernog kazeina u mlijeku zavisi od uslova sredine. Npr. ako mlijeko sadrži više kalcijuma biće manje monomera jer kalcijum djeluje polimerizaciono ili ako pretjerano razvodnjavamo mlijeko znatno će se povećati količina rastvorljivog kazeina. Ovo svjedoči da postoji reverzibilnost procesa prelaska monomera u polimjere i obrnuto.
Kazein se u mlijeku nalazi u polidisperznom stanju, što znači da njegove čestice imaju različitu veličinu. Prečnik micela varira od 30 do preko 300nm. Pod elektronskim mikroskopom izgledaju kao približno sferne čestice.
Na oblik kazeinske micele imaju uticaja faktori disperzne sredine. Npr. ako se mlijeko razblaži vodom pod elektronskim mikroskopom se može vidjeti da micele postaju ili razvučene iili se u vidnom polju javljaju kao veoma sitne tačke, dok krupne micele nestaju. Ako se zatim dodata voda ukloni ili se razblaženom mlijeku doda takva količina mlijeka da se postigne koncentracija kalcijuma koja je postojala u mlijeku prije razblaživanja, vidjeće se da su kazeinske micele opet poprimile sferni oblik i da im veličina odgovara onom u mlijeku. Ovo je dokaz da ![]() ima uticaja na veličinu i oblik kazeinskih micela.
ima uticaja na veličinu i oblik kazeinskih micela.
Ukoliko su čestice veće stabilnost kazeinskog rastvora je manja, pa faktori koji doprinose destabilizaciji sistema lakše izazivaju njegovu koagulaciju.
Pošto ![]() djeluje agregaciono samim tim on djeluje i destabilišuće. Agregacionim djelovanjem
djeluje agregaciono samim tim on djeluje i destabilišuće. Agregacionim djelovanjem ![]() objašnjava se pojava povećanja viskoziteta proizvoda, a u težim slučajevima do obrazovanja gela od mlijeka u toku skladištenja (npr. kod kondenzovanog i evaporisanog mlijeka). Ovo nastaje tako što se usljed isparavanja dijela vode iz mlijeka povećava koncentracija
objašnjava se pojava povećanja viskoziteta proizvoda, a u težim slučajevima do obrazovanja gela od mlijeka u toku skladištenja (npr. kod kondenzovanog i evaporisanog mlijeka). Ovo nastaje tako što se usljed isparavanja dijela vode iz mlijeka povećava koncentracija ![]() , a s tim u vezi povećavaju se kazeinske micele. Usljed isparavanja dijela vode kazeinske čestice su bliže jedna drugoj tako da električni naboj micele nije dovoljan da izvrši odbijanje uvećanih micela. Zbog ovoga dolazi do spajanja micela i u krajnjoj liniji do obrazovanja gela (Carić, Milanović, 1997).
, a s tim u vezi povećavaju se kazeinske micele. Usljed isparavanja dijela vode kazeinske čestice su bliže jedna drugoj tako da električni naboj micele nije dovoljan da izvrši odbijanje uvećanih micela. Zbog ovoga dolazi do spajanja micela i u krajnjoj liniji do obrazovanja gela (Carić, Milanović, 1997).
Istovremeno veća koncentracija ![]() neutrališe djelimično negativni naboj kazeina.
neutrališe djelimično negativni naboj kazeina. ![]() ima znatno manje u mlijeku pa je i njegova uloga manja.
ima znatno manje u mlijeku pa je i njegova uloga manja.
.
Sastav kazeinskog kompleksa
Kazein se u mlijeku nalazi u obliku Ca-soli. U njegov sastav ulaze i drugi sastojci kao što su Ca i Mg u obliku fosfata i citrata i K i Na u obliku jona i hlorida. Svi ovi sastojci obrazuju kazeinsku micelu bilo da je ona monomer ili da je nastala agregiranjem u čestice većih dimenzija.
Navedena vrijednost za Ca predstavlja zbir količina Ca:
- vezanog za proteinski dio kazeina. Dakle, to je dio koji obrazuje so Ca- kazeina. Preovlađuje gledište da je ovaj dio kalcijuma vezan za fosfornu kisleinu (organski fosfor), a ne za višak karboksilnih grupa aminokiselina.
- i neorganskog kalcijuma koji se nalazi u obliku soli fosforne kiseline (neorganski fosfor) i limunske kiseline.
Ca – fosfat je adsorbovan na površini kazeinskih čestica. Odnosno, obrazuje kompleksni jon sa Ca iz Ca-kazeinata (dakle, Ca koji je hemijski vezan sa organskim fosfatom).
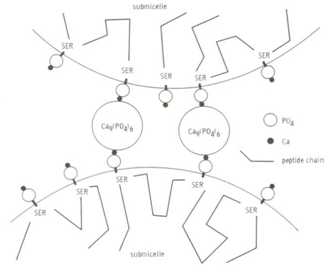
Do spajanja dvije micele dolazi preko kompleksa ![]() . Fosfatna grupa je vezana za alkoholnu grupu serina.
. Fosfatna grupa je vezana za alkoholnu grupu serina.
Slika 3. Veze između kazeinskih micela
Kazein je amfoteran (jer sadrži i ![]() i
i ![]() ) i za uslove mlijeka ima nešto kiseo karakter. Izoelektrična tačka kazeina je; pHIET = 4,6.
) i za uslove mlijeka ima nešto kiseo karakter. Izoelektrična tačka kazeina je; pHIET = 4,6.
Joni ![]() ili
ili ![]() neće izazvati spajanje monomera jer su ovi metali jednovalentni pa se drugi monomer ne može vezati. Zato se kaže da
neće izazvati spajanje monomera jer su ovi metali jednovalentni pa se drugi monomer ne može vezati. Zato se kaže da ![]() i
i ![]() djeluju stabilišuće (spriječavaju agregaciju, zauzmu mjesto Ca2+) na kazeinsku micelu.
djeluju stabilišuće (spriječavaju agregaciju, zauzmu mjesto Ca2+) na kazeinsku micelu.
Spisak korišćene literature možete naći u Literatura – Tehnologija mleka.