Prof. Dr Midhat Jašić
Tehnološki fakultet, Tuzla
Tel.: +387 61 721060; +387 35 320745
E-mail: jasic_midhat@yahoo.com
E-mail: midhat.jasic@untz.ba
.
.
Svrha dodavanja konzervansa je produženje održljivosti hrane i prevencija kvarenja odnosno mikrobiološke kontaminacije. Konzervansima se mogu smatrati sve tvari dodane u hranu koje sprečavaju rast ili uništavju mikroorganizame te inhibiraju enzimske i oksidacijske procese u hrani. Konzervansi mogu biti i tvari koje djeluju na smanjenje aktivnosti vode. Najpoznatiji tradicionalno korišten konzervans, koji je ujedno i najmanje opasan je kuhinjska sol, ali se ona ne smatra aditivom. Šećer i druga prirodna sladila dugo su tradicionalno kroz povijest korišteni kao konzervansi. Danas konzervans podsjeća na opasnost u hrani. U zdravstvenom pogledu rizične skupine konzervansa su nitriti i nitrati u mesu, benzojeva kiselina i njene soli u osvježavajućim pićima, sumpor dioksid u sušenim proizvodima od voća, sorbinska kiselina u proizvodima od voća i povrća i drugi.
Osobe koji se hrane salamurenim i dimljenim mesom moraju biti svjesne da će unijeti rizičniju količinu aditiva u obroku. U normalnim okolnostima i normalnim količinama konzumiranja ipak ne bi trebala imati štetnih efekata na zdravlje, ako se primjenjuje princip raznovrsne i umjerne prehrane. Hemijski konzervansi koji posjeduju antimikrobna svojstva vrlo su važna sredstva za čuvanje namirnica i njihovu sigurnost.
Biohemijski mehanizmi djelovanja konzervansa u hrani vrlo su raznoliki.Općenito mogu imati mikrobicidna, inhibicijska, antioksidativna i njima slična svojstva. Sa aspekta zdravstvene sigurnosti značajniji konzervansi koji se mogu naći u hrani su su: sulfiti i sumpor dioksid, soli nitrita i nitrata, benzojeva kiselina, sorbinska kiselina, octena kiselina, propionska kiselina, gliceril esteri, p-hidroksibenzoat alkil esteri, epoksidi, antibiotici. Neki od njih opisani su u ovom poglavlju.
Sulfiti i sumpor dioksid. Sumpor dioksid i njegovi derivati dugo se koriste u zaštiti namirnica. Dodaju se u hranu u svrhu inhibiciji i kontroli rasta mikroorganizama, sprječavanja neenzimskog posmeđivanja, inhibicije reakcija kataliziranih enzimima te kao antioksidanti i reducirajuća sredstva. Sumpordioksid ( SO2 ) i njegovi derivati metaboliziraju se do sulfata i izlučuju u urin bez vidljivih patoloških efekata. Međutim, zbog ozbiljnih reakcija koje na SO2 i derivate pokazuju osjetljiviji astmatičari, njegova upotreba u hrani podvrgnuta je strogim mjerama informiranja potrošača. Bez obzira na to, ovi konzervansi imaju važnu ulogu u čuvanju poluproizvoda.
U prehrambenoj industriji primjenjuju se najčešće u obliku plinovitog SO2, te natrijevih, kalijevih ili kalcijevih soli sulfita (SO32-), bisulfita (HSO3-) ili metabisulfita (S2O52-). Najčešće se koriste natrij i kalij metabisulfit jer u čvrstim supstancama pokazuju veliku stabilnost na autooksidaciju. Plinoviti SO2 koristi se kada luženje čvrstih supstanci može uzrokovati probleme, gdje služi i kao kiselo sredstvo za kontrolu pH. Kalijev metabisulfit – “vinobran”-najčešće korišteni oblik sumpora posebno u manjim podrumima. Kao produkt tokom njegovog otapanja u vodi nastaje sumporasta kiselina – spoj sumpornog dioksida i vode. U praksi se koristi i tekući sumporni dioksid (sprej). Prednost ovog oblika sumpora ogleda se u preciznijem doziranju.U primjeni su i sumporne trake. Na traci se nalazi čisti sumpor koji se paljenjem trake razvija u sumporni dioksid. Ova forma uglavnom se koristi za sumporenje bačavi.
Sumpor dioksid je vjerojatno najefikasniji danas poznati inhibitor neenzimskog posmeđivanja. Inhibicija neenzimskog posmeđivanja uključuje veliki broj hemijskih mehanizama od kojih je najvažnija reakcija sumpor (IV) oksoaniona (bisulfit) s karbonilnim skupinama reducirajućih šećera i drugih sastojaka koji sudjeluju u posmeđivanju. Sumpor dioksid inhibira i neke enzimski katalizirane reakcije, posebno enzimsko posmeđivanje, koje su važne u čuvanju namirnica. Proizvodnja smeđih pigmenata enzimski kataliziranom oksidacijom fenolnih spojeva može dovesti do značajnih poremećaja u kakvoći tokom prerade svježeg voća i povrća. Bilo kako bilo, upotreba sprejeva ili otopina na bazi sulfita ili metabisulfita sa ili bez limunske kiseline efikasna je u kontroli enzimskog posmeđivanja u oguljenim i narezanim rajčicama, mrkvi i jabukama.
Sumpor dioksid u nekim namirnicama djeluje i antioksidativno. To mu nije primarna funkcija. Kada se dodaje u pivo, značajno smanjuje razvoj «oksidativnih» okusa tokom skladištenja. Crvena boja svježeg mesa može se uspješno održavati pomoću sumpor dioksida, ali to nije dopušteno zbog mogućnosti maskiranja kvarenja i zloupotrebe na mesnim proizvodima.
U proizvodnji tijesta od pšeničnog brašna sumpor dioksid utječe na reverzibilno cijepanje disulfidnih veza u proteinima. U proizvodnji kolačića smanjuje vrijeme miješanja i elastičnost tijesta koje omogućuje njegovo razvlačenje, te smanjuje razlike kod upotrebe različitih šarži brašna.
Plinoviti sumpor dioksid nanosi se na voće prije sušenja, često u prisustvu sredstava za puferiranje (npr. NaHCO3). Ovim postupkom sprječava se posmeđivanje i potiče izbjeljivanje pigmenata na bazi antocijana. Postignuta svojstva poželjna su u proizvodima poput bijelog vina i maraskino višanja.
Soli nitrita i nitrata. Kalijeve i natrijeve soli nitrita i nitrata često se koriste u smjesama za salamurenje mesa u svrhu razvoja i očuvanja boje, inhibicije mikroorganizama i razvoja karakteristične arome. Nitriti imaju jače izražena funkcionalna svojstva od nitrata. U mesu nitriti stvaraju dušikov oksid koji reagira sa hemom tvoreći nitrozomioglobin, pigment odgovoran za crvenu boju usalamurenog mesa. Senzorsko ocjenjivanje pokazuje da nitriti doprinose i okusu usalamurenog mesa, očito zbog antioksidativne uloge. Nadalje, nitriti inhibiraju razvoj klostridija u usitnjenom konzerviranom i usalamurenom mesu. Kada se koriste u ovu svrhu, nitriti su efikasaniji pri pH 5,0 – 5,5 nego pri višim pH vrijednostima.
U nekim vrstama salamurenog mesa, a pomoću crijevne mikroflore nitriti sudjeluju u stvaranju malih količina toksičnih nitrozamina.
Nitratne soli prirodno su prisutne u velikom broju namirnica, uključujući i povrće poput špinata. Nakupljanje velikih udjela nitrata u biljkama uzgajanim na jako gnojenim površinama pobuđuje veliko zanimanje, naročito ako su namijenjene za proizvodnju dječje hrane. Redukcija nitrata u nitrite u crijevima uz naknadnu apsorpciju može uzrokovati cijanozu zbog sinteze methemoglobina. Zbog toga je upotreba nitrita i nitrata u hrani upitna.
Antimikrobna svojstva nitrita u salamurenom mesu opravdavaju njegovu upotrebu, naročito kada postoji mogućnost razvoja Clostridium botulinuma. Međutim, u namirnicama u kojima ne postoji opasnost od botulizma postoji slabo opravdanje za njihovu primjenu.
Benzojeva kiselina. Benzojeva kiselina (C6H5COOH) ima široku primjenu kao antimikrobno sredstvo u hrani, a prirodno je prisutna u brusnicama, šljivama, cimetu i klinčiću. Nedisocirana kiselina ima antimikrobnu aktivnost, a optimalni pH kreće se između 2,5 i 4,0. Prikladna je za upotrebu u voćnim sokovima, gaziranim pićima, kiselim krastavcima i kiselom zelju. Natrij benzoat je topljiviji u vodi od same kiseline i češće se koristi. U proizvodu jedan dio soli prelazi u aktivni kiseli oblik, koji je najdjelotvorniji protiv kvasaca i bakterija. Manje je djelotvoran na plijesni. Često se benzojeva kiselina primjenjuje u kombinaciji sa sorbinskom kiselinom ili parabenima, a maseni udjeli u kojima se primjenjuje kreću se između 0,05 i 0,1 %.
Kada se unosi u količinama definiranim prema ADI vrijednostima, benzojeva kiselina nije štetna za ljudski organizam. Brzo se izlučuje iz tijela prvenstveno nakon konjugacije s glicinom dajući hipurnu kiselinu (benzoil glicin). Ovaj korak detoksikacije sprječava akumulaciju benzojeve kiseline u tijelu.Ipak sa konzumacija spojeva koji sadrže benzolovu jezgru.- oprez i predostrožnost, naročito u količinama.
Sorbinska kiselina. Ravnolačane, monokarboksilne, alifatske masne kiseline imaju antimikotičnu aktivnost, a naročito efikasni su analozi α-nezasićenih masnih kiselina. Sorbinska kiselina i njene natrijeve i kalijeve soli imaju široku primjenu u inhibiciji plijesni i kvasaca u velikom broju namirnica poput sira, pekarskih proizvoda, voćnih sokova, vina i kiselih krastavaca. Sorbinska kiselina naročito je efikasna u sprječavanju razvoja plijesni te malo doprinosi okusu u koncentracijama ispod 0,3 %. Primjena može biti direktna, u vidu površinskih premaza, ili inkorporiranjem u omotače. Aktivnost sorbinske kiseline povećava se sa smanjenjem pH, ukazujući da je nedisocirani oblik aktivniji od disociranog. Općenito, sorbinska kiselina je efikasna do pH 6,5, koji je znatno viši od efikasnog raspona pH za propionsku i benzojevu kiselinu.
Antimikotična aktivnost sorbinske kiseline raste jer plijesni ne mogu metabolizirati α-nezasićenu diensku komponentu alifatskoga lanca. Smatra se da se dienska struktura sorbinske kiseline upliće sa staničnim dehidrogenazama koje dehidrogeniraju masne kiseline u prvom stupnju oksidacije. Zasićene kratkolančane (C2 – C12) masne kiseline imaju umjerenu inhibicijsku aktivnost na plijesni poput Penicilliuma. Međutim, neke od ovih plijesni mogu posredovati u ß-oksidaciji zasićenih masnih kiselina do odgovarajućih ß-keto kiselina, posebno kada su kiseline prisutne u graničnom udjelu aktivnosti. Dekarboksilacijom nastalih ß-keto kiselina nastaju odgovarajući metil ketoni koji nemaju antimikrobna svojstva. Neke plijesni mogu metabolizirati i sorbinsku kiselinu, vjerojatno ß-oksidacijom, slično sisavcima. Svi pokazatelji ukazuju da ljudi i životinje metaboliziraju sorbinsku kiselinu na isti način kao i prirodno prisutne masne kiseline.
Iako se sorbinska kiselina na prvi pogled čini stabilnom i nereaktivnom, u hrani je često mikrobiološki ili hemijski promijenjena. Ako vino koje sadrži sorbinsku kiselinu podlegne kvarenju u boci pod utjecajem bakterija mliječne kiseline, razvit će se neugodan naknadni okus koji podsjeća na pelargonije. Bakterije mliječne kiseline reduciraju sorbinsku kiselinu do sorbinskog alkohola, a zatim, zbog kiselih uvjeta koje same stvaraju, uzrokuju njegovo prevođenje u sekundarni alkohol. Konačna reakcija je tvorba etoksiliranog heksadiena koji ima izraženu, prepoznatljivu aromu po pelargonijama.
Sorbinska kiselina može se koristiti i u kombinaciji sa sumpor dioksidom, što vodi do reakcija koje uključuju i sorbinsku kiselinu i sumpor (IV) oksoanione.
Iako su sorbinska kiselina i kalij sorbat već dugo poznati kao antimikotici, novija istraživanja pokazuju da sorbat ima široku antimikrobnu aktivnost koja obuhvaća mnoge bakterijske vrste koje uzrokuju kvarenje svježeg mesa i ribe. Posebno je efikasan u usporavanju sinteze toksina Clostridium botulinuma u slanini i svježoj hlađenoj ribi pakiranoj u modificiranoj atmosferi.
Octena-sirćetna kiselina. Konzerviranje hrane pomoću octene-sirćetna kiseline (CH3COOH) poznata je još od davnina. Osim octa (4 % octena kiselina) i octene kiseline, u zaštiti namirnica koriste se i odgovarjuće soli.
Octena kiselina i njene soli kao konzervansi
| rb | Naziv spoja | Hemijska formula |
| 1. | natrij acetat | CH3COONa |
| 2. | kalij acetat | CH3COOK |
| 3. | kalcij acetat | (CH3COO)2Ca |
| 4. | natrij diacetat | CH3COONa × CH3 – COOH × ½ H2O |
Soli se koriste u kruhu i drugim pekarskim proizvodima (0,1 – 0,4 %) u svrhu sprječavanja nitavosti kruha i razvoja plijesni bez utjecaja na kvasce. Octena kiselina koristi se u ukiseljenim mesnim i ribljim proizvodima. Ako su prisutni fermentabilni ugljikohidrati, mora biti prisutno barem 3,6 % octene kiseline kako bi se spriječio rast mliječnih bakterija i kvasaca. Octena kiselina koristi se i u kečapu, majonezi, kiselim krastavcima, gdje ima dvostruku ulogu: inhibicija mikroorganizama i doprinos okusu. Antimikrobna aktivnost octene kiseline povećava se sa smanjenjem pH, po čemu je slična drugim alifatskim masnim kiselinama.
Propionska kiselina. Propionska kiselina (CH3-CH2-COOH) te njene natrijeve i kalcijeve soli antimikrobno djeluju na plijesni i neke bakterije. Ovaj spoj prirodno je prisutan u siru ementaleru (do 1 % mase), gdje ga proizvodi Propionibacterium shermanii. Propionska kiselina intenzivno se koristi u pekarstvu gdje, ne samo da efikasno inhibira razvoj plijesni, nego i Bacillus mesentericus, koji uzrokuje nitavost kruha. Najčešće se koristi u udjelima 0,3 % mase. Kao i kod drugih antimikrobnih sredstava na bazi karboksilnih kiselina, aktivan je nedisocirani oblik propionske kiseline, a u većini primjena raspon aktivnosti je do pH 5,0. Toksičnost propionske kiseline za plijesni i bakterije povezana je s nemogućnošću tih mikroorganizama da metaboliziraju okosnicu građenu od tri C-atoma.
Sisari propionsku kiselinu metaboliziraju slično kao i ostale masne kiseline, pa u udjelima u kojima se koristi nije toksična za ljude.
Gliceril esteri. Veliki broj masnih kiselina i monoglicerida posjeduje izraženu antimikrobnu aktivnost na gram-pozitivne bakterije i neke kvasce. Nezasićene kiseline, posebno one sa 18 ugljikovih atoma jako su aktivne kao kiseline, dok su srednjelančane kiseline (12 C-atoma) najefikasnije kada su esterificirane s glicerolom. Gliceril monolaurat (II) u udjelima 15 – 250 ppm inhibicijski djeluje na neke potencijalno patogene stafilokoke i streptokoke. Često se upotrebljava u kozmetici, a zbog lipidne prirode i u nekim namirnicama.
Lipofilna sredstva ove vrste inhibicijski djeluju i na C. botulinum, pa se u ovu svrhu gliceril monolaurat može koristiti u usoljenom mesu i hlađenoj pakiranoj svježoj ribi. Inhibicijski efekat lipofilnih derivata glicerida leži u njihovoj sposobnosti prijenosa protona kroz staničnu membranu čime se efikasno uništava pokretačka sila protona potrebna za transport supstrata. Uništavanje staničnog zida javlja se samo pri vrlo visokim koncentracijama sredstva, a smrt je posljedica stvaranja šupljina u staničnoj stjenci.
Parabeni , p-Hidroksibenzoat alkil esteri. To su skupina alkil estera p-hidroksibenzojeve kiseline (pHBA) koji se koriste kao antimikrobna sredstva u hrani, farmaceutskim proizvodima i kozmetici. Metil (III), propil i heptil (IV) esteri koriste se u domaćinstvima, a u nekim zemljama u domaćinstvu se koriste i etil i butil esteri. Kao konzervansi koriste se u pekarskim proizvodima, bezalkoholnim pićima, pivu, maslinama, kiselim krastavcima, džemovima, želeima i sirupima.
Na aromu utječu vrlo malo, efikasni su inhibitori plijesni i kvasaca (0,5 – 0,1 % masenih), relativno su nedjelotvorni na bakterije, posebno na gram-negativne bakterije. S povećanjem duljine alkilnog lanca povećava se njihova antimikrobna aktivnost, a smanjuje topljivost u vodi. Češće se koriste parabeni kraćeg lanca jer su topljiviji. Za razliku od ostalih antimikotičkih sredstava, parabenisu aktivni pri pH 7 i više, očito zbog sposobnosti da u tom stanju ne disociraju. Fenolne skupine daju im slabo kisela svojstva. Esterska veza otporna je na hidrolizu čak i na temperaturama sterilizacije. Po mnogim svojstvima parabeni su slični benzojevoj kiselini, pa se često i primjenjuju zajedno. Parabeni su slabo toksični za ljude i izlučuju se urinom nakon hidrolize esterskih skupina i naknadne metaboličke konjugacije.
Epoksidi. Većina antimikrobnih sredstava koja se primjenjuju u hrani u udjelima u kojima se primjenjuju ima inhibicijsko, a ne uništavajuće djelovanje. Izuzetak su etilen i propilen oksidi. Ova hemijska sredstva za sterilizaciju primjenjuju se u tretiranju namirnica niske vlažnosti i sterilizaciji materijala za aseptično pakiranje. Kako bi kontakt s mikroorganizmima bio što veći, epoksidi se nanose u plinovitom stanju, a nakon prikladnog vremena izlaganja višak epoksida ispire se ili razrjeđuje.
Epoksidi su reaktivni ciklički esteri koji uništavaju sve oblike mikroorganizama, uključujući spore i viruse. Mehanizam njihovog djelovanja još nije razjašnjen. Za etilen oksid smatra se da se letalni efekt postiže alkilacijom esencijalnih intermedijarnih metabolita koji imaju hidroksietilnu skupinu (–CH2–CH2–OH). Epoksidi reagiraju s vodom dajući odgovarajuće glikole. Međutim, toksičnost glikola vrlo je niska, pa stoga ne pridonose inhibicijskom utjecaju.
Aktivni oblik epoksida uklanja se iz tretiranih namirnica. Glikoli nastali razrjeđivanjem s vodom posjeduju malu toksičnost, pa se čini da se plinovita sredstva za sterilizaciju mogu koristiti u velikoj mjeri. Međutim, njihova upotreba ograničena je na suhe namirnice, poput jezgarastog voća i začina. Reakcija s vodom brzo smanjuje koncentraciju epoksida u namirnicama s visokim udjelom vode. Začini uglavnom sadrže visok broj mikroorganizama i namijenjeni su za upotrebu u pokvarljivim namirnicama. Termička sterilizacija začina nije prikladna jer su važni sastojci arome hlapljivi te je proizvod nestabilan na visokim temperaturama. Stoga je tretiranje epoksidima pogodno za smanjenje broja mikroorganizama.
Kod uporabe epoksida treba imati na umu mogućnost stvaranja relativno toksičnih klorhidrina koji su rezultat reakcije epoksida i anorganskih klorida. Međutim, postoje izvješća da dijetalni klorhidrin u niskim koncentracijama nema patološko djelovanje. Drugi predmet razmatranja upotrebe epoksida treba biti mogućnost nepovoljnog djelovanja na vitamine, uključujući riboflavin, niacin i piridoksin.
Antibiotici. Antibiotici su velika skupina antimikrobnih spojeva koje proizvode mikroorganizmi. Imaju selektivnu antimikrobnu aktivnost, te je njihova primjena u medicini značajno doprinijela u polju kemoterapije. Uspješnost antibiotika u kontroli patogenih mikroorganizama na živim životinjama dovela je do intenzivnih istraživanja o mogućnosti njihove primjene u čuvanju namirnica. Međutim, zbog straha od razvoja rezistentnih sojeva mikroorganizama uslijed ekstenzivne upotrebe antibiotika, njihova upotreba, uz iznimku nizina, nije trenutno dopuštena. Ako se antibiotik predložen za upotrebu na namirnicama koristi i u medicinske svrhe, posebnu pažnju treba posvetiti mogućnosti razvoja rezistentnih sojeva mikroorganizama. Primjer korištenihantibiotika kao konzervansa je nizin, polipeptidni antibiotik kojega proizvode mliječni streptokoki. Nizin se koristi za sprječavanje kvarenja mliječnih proizvoda, poput sira i kondenziranog mlijeka u svrhu sprječavanja prevelikog rasta C. botulinuma. Aktivan je protiv gram-pozitivnih mikroorganizama, naročito u sprječavanju rasta spora i ne koristi se u medicini. Nizin ne djeluje na gram-negativne mikroorganizme koji uzrokuju kvarenje, a otporni su i neki sojevi klostridija. Za ljude nizin nije toksičan, ne uzrokuje otpornost na druge antibiotike i razgrađuje se u probavnom traktu bez štetnih posljedica.
Neke zemlje dopuštaju i upotrebu nekih drugih antibiotika, poput klortetraciklina i oksitetraciklina. Većina sadašnje primjene antibiotika odnosi se na njihovu upotrebu kao dodataka drugim metodama konzerviranja. Ponajprije se to odnosi na usporavanje kvarenja lako pokvarljive hrane koja se čuva u hladnjaku i smanjenje oštrine termičkih procesa. Svježe meso i riba lako su pokvarljivi proizvodi u kojima bi upotreba antibiotika bila izrazito povoljna.
Antioksidanti. Oksidacija je proces otpuštanja elektrona s atoma ili skupine atoma. Istovremeno se odvija i odgovarajuća reakcija u kojoj se elektroni vežu na drugi atom ili skupinu atoma. Reakcije oksidacije mogu, ali ne moraju, uključivati i vezanje kisika ili otpuštanje vodika sa čestice koja se oksidira. Oksido-redukcijske reakcije česte su, kako u biološkim sistemima, tako i u hrani. Iako su neke oksidacijske reakcije u hrani poželjne, neke mogu uzrokovati štetne posljedice, poput degradacije vitamina, pigmenata i lipida, uz gubitak nutritivne vrijednosti i razvoja naknadnog okusa. Kontrola nepoželjnih reakcija oksidacije u hrani uglavnom se postiže primjenom procesa i tehnika pakiranja koje isključuju kisik ili uključuju dodavanje prikladnih hemijskih sredstava.
Prije razvoja specifičnih hemijskih tehnologija za kontrolu oksidacije lipida mehanizmom slobodnih radikala, pojam antioksidans odnosio se na sve sastojke koji su inhibirali reakcije oksidacije bez obzira na mehanizam. Na primjer, askorbinska kiselina smatrala se antioksidantom i koristila se u sprječavanju enzimskog posmeđivanja na površini rezanog voća i povrća. Kod ove primjene askorbinska kiselina djeluje kao reducirajuće sredstvo prenoseći atome vodika natrag na kinone koji se stvaraju enzimskom oksidacijom fenolnih spojeva. U zatvorenim sistemima askorbinska kiselina reagira s kisikom i djeluje kao sredstvo za vezanje kisika. Slično, sulfiti se u sistemu hrane oksidiraju do sulfonata i sulfata te tako djeluju kao efikasni antioksidanti u namirnicama poput sušenoga voća. Kao antioksidanti u hrani najčešće se koriste fenolni spojevi. U novije vrijeme pojam «prehrambeni antioksidans» odnosi se na one spojeve koji ometaju lančanu reakciju oksidacije lipida i one koji vezuju singlet kisik, međutim pojam se ne bi smio koristiti u tako uskom smislu.
Antioksidanti uglavnom imaju različitu efikasnost u zaštiti hrane, a njihovom se kombinacijom postiže bolja efikasnost u odnosu na pojedinačnu upotrebu. Smjesa antioksidanata može imati sinergistički efekat. Ipak mehanizmi takvog djelovanja još nisu razjašnjeni.Vjerojatno da askorbinska kiselina regenerira fenolne antioksidante nadomještanjem vodikovih iona na fenolne radikale koji se formiraju reakcijom u kojoj fenolni antioksidanti daju vodik u lančanu reakciju lipidne oksidacije. Kako bi se postigla ova aktivnost, mora se smanjiti polarnost askorbinske kiseline da bi ona bila topljiva u mastima. To se postiže esterifikacijom masnih kiselina kojom se dobivaju spojevi poput askorbil palmitata.
Prisutnost prijelaznih metala, naročito bakra i željeza, potiče oksidaciju lipida djelujući poput katalizatora. Ovi metalni prooksidanti inaktiviraju se sredstvima za heliranje, poput limunske kiseline i EDTA. Kada se koriste na ovaj način, helirajuća sredstva smatraju se i sinergistima jer u velikoj mjeri utječu na aktivnost fenolnih antioksidanata. Međutim, kada se samostalno primjenjuju, nemaju antioksidativno djelovanje.
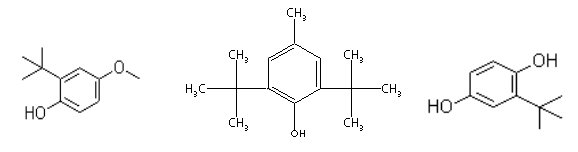
Veliki broj prirodnih sastojaka posjeduje antioksidativna svojstva, a poesbno treba istaći tokoferole, koji se često koriste. Kao efikasna antioksidativna sredstva upotrebljavaju se ekstrakti začina, naročito ruzmarina. Ostali prirodni antioksidanti su koniferil alkohol (prisutan u biljkama) te gvajakonska i gvajanska kiselina iz gume guaiac. Ovi spojevi strukturno su slični butiliranom hidroksianisolu (BHA), butiliranom hidroksitoluenu (BHT), propil galatu, te di-t-butilhidrokinonu (TBHQ), koji su sintetski antioksidanti, odobreni za uporabu u namirnicama.
Nordihidrogvajaretična kiselina, spoj sličan nekim sastojcima gume gvajak, efikasni je antioksidans, no njena je izravna upotreba u namirnicama zabranjena zbog toksičnog djelovanja. Svi ovi fenolni spojevi djeluju kao sredstva za usporavanje oksidacije, sudjelujući u reakcijama nizom slobodnih radikala stabiliziranih rezonancijom, no vjeruje se da djeluju i kao sredstva za vezanje singlet kisika. Međutim, smatra se da je ß-karoten efikasniji u vezanju singlet kisika od fenolnih spojeva.
Sredtva za zaštitu od kisika. Kisik je jedan od faktora koji utječe na mnogobrojne procese kvarenja hrane. Ukoliko se smanji količina kisika u atmosveri gdje se čuva hrana procesi kvarenja se mogu usporiti. Neki procesi uklanjanja kisika uključuju upotrebu inertnih plinova poput dušika i ugljičnog dioksida kojima se popunjava atmosfera u pakovanju namirnice. Proizvod koji je potpuno odzračen, «ispran» dušikom i hermetički zatvoren je otporniji na oksidativno kvarenje ,jer mu se u okolnoj atmosveri znatno smanjuje sadržaj kisika.
.
Procesni aditivi
Procesin aditivi se dodaju tokom skladištenja, prerade i pakovanja hrane. Većina aditiva se dodaju tokom prerade a neki od njih su tipičn jer mogu bitno utjecati na promjena proizvoda i procesa. To mogu biti sredstva protiv grudvanja praškastih materijala, emulgatori, helirajući agensi, stabilizatori,humektanti, puferi , sredstva za bistrenje i zamućivanje tekućina, sredtva za izbjeljivanje, klizna sredstva te sredstva za pahu1jčenje.
Po hemijskom sastavu ovi aditivi mogu biti kiseline, baze soli, odnosno puferski sistemi, Ovu kategoriju aditiva uvodimo i radi lakše sistematizacije i dobijanja kvalitetnije predodžbe o aditivima.
Aditiv ima uvijek više od jednog funkcionalnog svojstva, tako da njegovo dodavanje u hranu tokom procesa može uzrokovati višestruke promjene.
.
Soli kao aditivi
Tipični primjeri korištenja soli kao aditiva su u procesima proizvodnje mliječnih proizvoda, preradi mesa ( fosfati) kao i helata.
Soli u mliječnim proizvodima. Soli se mnogo koriste u proizvodnji sireva i zamjena za sir u cilju postizanja ravnomjerne i meke teksture. Ovi aditivi nekada se nazivaju i soli za emulgiranje jer imaju sposobnost povećanja disperzivnosti masti. Soli koje se koriste u proizvodnji sira su mono-, di- i trinatrij fosfat, dikalijfosfat, natrij heksametafosfat, natrij hidrogen pirosfat, tetranatrij pirofosfat, natrij aluminij fosfat i ostali kondenzirani fosfati, trinatrij citrat, trikalij citrat, natrij tartarat i kalij natrij tartarat.
Fosfati i vezivanje vode u tkivima animalnog porijekla. Dodatak prikladnih fosfata povećava kapacitet vezanja vode sirovog i termički tretiranog mesa, pa se koriste u proizvodnji kobasica, u salamurenju šunke, te u smanjenju gubitka vlage peradi i plodova mora. Najčešće se u procesirano meso i plodove mora dodaje natrij tripolifosfat. Često se koristi i u smjesi s natrij heksametafosfatom kako bi se povećala otpornost na kalcijeve ione prisutne u salamuri koja se koristi za salamurenje mesa. Orto- i pirofosfati često precipitiraju ako se koriste u salamuri sa velikim udjelom kalcija.
Unatoč intenzivnim istraživanjima, mehanizam kojim alkalni fosfati i polifosfati povećavaju hidrataciju mesa još uvijek nije razjašnjen. Proces može uključivati utjecaj promjene pH utjecaj ionske jakosti te specifične interakcije fosfatnih aniona s divalentnim kationima i miofibrilarnim proteinima. Mnogi vjeruju da je glavna funkcija fosfata kompleksiranje kalcija i mekšanje (labavljenje) strukture tkiva koje je rezultat reakcije s kalcijem. Također se vjeruje da vezanje fosfatnih aniona na proteine i simultano cijepanje unakrsnih veza između aktina i miozina rezultira povećanim elektrostatskim odbijanjem između peptidnih lanaca i bubrenjem sistema mišića. Ako je u okolini dostupna voda, olabavljena mreža proteina može je veže u imobiliziranom stanju. Nadalje, zbog povećanja ionske snage, interakcije među proteinima vjerojatno se smanjuju do tačke u kojoj dio miofibrilarnih proteina stvara koloidnu otopinu. U proizvodima od miješanog mesa, kakve su kobasice i mortadela, dodavanje natrij klorida (2,5 – 4,0 %) i polifosfata (0,35 – 0,5 %) doprinosi stabilizaciji emulzije, te koheziji koaguliranih proteina nakon kuhanja.
Ako se otapanje potaknuto fosfatima odvija prvenstveno na površini tkiva, kao što je slučaj sa filetima ribe, školjkama i peradi potopljenima u polifosfatne otopine (6 – 12 % otopina s 0,35 – 0,5 % retencijom), tokom kuhanja stvara se sloj koaguliranih proteina, te se povećava zadržavanje vlažnosti.
Sredstva za helatizaciju-sekvestranti. Sredstva za helatizaciju ili sekvestranti igraju važnu ulogu u stabilizaciji hrane zahvaljujući reakcijama s metalnim i zemnoalkalijskim ionima s kojima stvaraju komplekse koji mijenjaju svojstva iona i njihov utjecaj na hranu. Velik broj sredstava za helatizaciju koja se koriste u prehrambenoj industriji su prirodne materije, poput polikarboksilnih kiselina (limunska, jabučna, vinska, oksalna, sukcinska kiselina), polifosfatnih kiselina (adenozin trifosfat i pirofosfat) te makromolekula (porfirini, proteini). Mnogi metali se u prirodi nalaze u helatnom obliku. Kao primjeri mogu se navesti magnezij u hlorofilu, bakar, cink i mangan u enzimima, željezo u proteinima poput feritina, željezo u porfirinskom prstenu mioglobina i hemoglobina. Kada se ovi ioni oslobode hidrolitičkim ili drugim degraditivnim reakcijama, mogu sudjelovati u reakcijama koje vode do obezbojenja, oksidativne užeglosti, mutnoće, te promjena arome u hrani. Sredstva za helatizaciju se dodaju kako bi stvarala komplekse s ovim ionima i tako stabilizirala namirnicu.
Svaka molekula ili ion s dva nesparena elektrona može stvarati komplekse ili koordinativnu vezu s ionima metala. Stoga, čestice koje sadrže dvije funkcionalne skupine poput -OH, -SH, -PO3H2, C=O, -NR2, -S- i -O- u pogodnom geometrijskom odnosu, može stvarati helate s metalima u prikladnom fizikalnom okruženju. Limunska kiselina i njeni derivati, različiti fosfati i soli EDTA najčešće su korištena sredstva za helatizaciju.
Na stvaranje jakih metalnih helata, osim steričkih i elektronskih faktora, utječe i pH.
Sredstva za helatizaciju nisu antioksidanti u smislu da sprječavaju oksidaciju lančanom reakcijom ili vezanjem kisika. Međutim, značajni su kao antioksidativni sinergisti jer uklanjaju ione metala koji kataliziraju reakcije oksidacije. Pri odabiru sredstva za helatizaciju koje će se koristiti u svrhu antioksidativnog sinergističkog učinka, treba voditi računa o njegovoj topljivosti. Limunska kiselina i citratni esteri (20 – 200 ppm) u otopini propilen glikola topljivi su u mastima i uljima te su stoga efikasni sinergisti u lipidnim sistemima. S druge strane, Na2EDTA i Na2Ca-EDTA topljivi su samo djelomično, pa nisu efikasni u lipidnim sistemima. Soli EDTA (do 500 ppm), međutim, vrlo su efikasni antioksidanti u emulzijama kakvi su preljevi za salate, majoneza, margarin, jer tu mogu djelovati u vodenoj fazi.
Iako se limunska i fosfatna kiselina koriste kao sredstva za zakiseljavanje u bezalkoholnim pićima, one također helatiziraju metale koji bi inače uzrokovali oksidaciju materije arome, poput terpena, te uzrokovali reakcije obezbojenja. Sredstva za helatizaciju također stabiliziraju fermentirana sladna pića kompleksiranjem bakra. Slobodni bakar katalizira oksidaciju polifenolnih spojeva, koji zatim reagiraju s proteinima i uzrokuju trajno tamnjenje ili mutnoću.
.
Kiseline kao aditivi
Organske i anorganske kiseline često su prisutne u hrani gdje mogu imati veći broj funkcija, od intermedijarnih metabolita do sastojaka puferskih sistema. Jedna od izuzetno značajnih funkcija kiselina je regulacija pH vrijednosti hrane. Pri smanjenoj vrijednosti pH, odnosno u kiselim sredinam inhibira se rast većine mikroorganizama. Zbog toga se kiseline i njihove soli primjenjuju se za sprječavanju mikrobiološkog kvarenja (npr. sorbinska i benzojeva kiselina) u konzerviranju namirnicaOsim toga kiseline s primjenjuju u hemijskim sredstvima za dizanje tijesta, kao helatna sredstva, zaatim za stvaranje pektinskih gelova, kao sredstva za sprječavanje pjenjenja.
Jedna od najvažnijih uloga kiselina u hrani je sudjelovanje u puferskim sistemima.
Kiseline, poput limunske, dodaju se umjereno kiselom voću i povrću kako bi im se pH snizio na vrijednosti niže od 4,5. U proizvodnji konzervirane hrane to omogućuje provođenje sterilizacije u nešto blažim uvjetima, i time se sprječava razvoj štetnih mikroorganizama (npr. Clostridium botulinum).
Veliki broj organskih kiselina može se koristiti u proizvodnji hrane.
| rb | Naziv spoja | Hemijska formula |
| octena | (CH3COOH), | |
| mliječna | (CH3-CHOH-COOH), | |
| limunska | [HOOC-CH2COH(COOH)-CH2-COOH], | |
| maleinska | (HOOC-CHOH-CH2-COOH), | |
| fumarna | (HOOC-CH=CH-COOH), | |
| sukcinska | (HOOC-CH2-CH2-COOH) i | |
| vinska | (HOOC-CHOH-CHOH-COOH). |
Fosfatna kiselina je jedina anorganska kiselina koja se često koristi u zakiseljavanju hrane. Ona je važno sredstvo za zakiseljavanje gaziranih pića, naročito kole. Druge mineralne kiseline (HCl, H2SO4) uglavnom prejako disociraju za namjenu u prehrani, pa njihova primjena može dovesti u pitanje kvalitetu hrane.
Tabela: Neke od najčešće korištenih organskih kiselina
| rb | Naziv spoja | Hemijska formula |
| Fosfatna kiselina | H3PO4 | |
| Hlorovodonična | HCl | |
| Sumorna i sumorasta | H2SO4 |
.
Baze kao aditivi
Bazne ili alkalne materije imaju veliki broj namjena u hrani i prehrambenoj industriji. Većina primjena baza podrazumijeva puferiranje i prilagodbu pH. Ostale funkcije su stvaranje CO2, poboljšanje boje i arome, otapanje proteina i hemijsko guljenje.
Neki prehrambeni proizvodi tretiraju se lužinama u svrhu poboljšanja boje i arome. Tako se zrele masline tretiraju otopinom NaOH kako bi se uklonila gorčina i razvila tamnija boja. Pereci se potapaju u otopinu 1,25 % NaOH prije pečenja, u svrhu modifikacije škroba i proteina, stvaranja glatke površine i tamno smeđe boje tokom pečenja. U pripremi tijesta za tortille vrši se tretiranje s NaOH. U obradi kakao zrna za proizvodnju tamne čokolade najčešće se koristi kalij karbonat. Povišeni pH pospješuje reakcije posmeđivanja između šećera i aminokiselina i polimerizaciju flavonoida, rezultirajući glatkijim, manje kiselim i manje gorkim okusom čokolade, tamnijom bojom i nešto boljom topljivošću.
Prehrambeni sistemi nekada zahtijevaju podešavanje pH na više vrijednosti, kako bi im se povećala stabilnost i poboljšala svojstva. Na primjer, alkalne soli poput dinatrij fosfata, trinatrij fosfata i trinatrij citrata koriste se u proizvodnji sira (1,5 – 3 %) kako bi se povisio pH (sa 5,7 na 6,3) i utjecalo na disperziju proteina (kazeina). Interakcije sol–protein poboljšavaju emulgiranje i sposobnost proteina sira da vežu vodu tako što se soli vežu na kalcij kazeinskih micela tvoreći helate.
Dodatak fosfata i citrata mijenja odnos soli u krajnjem mliječnom proizvodu stvaranjem kompleksa s ionima kalcija i magnezija iz kazeina.
Jake baze primjenjuju se u guljenju različitog voća i povrća. Izlaganje proizvoda vrućim otopinama natrij hidroksida. Uz naknadnu blagu abraziju dovodi do guljenja kožice uz smanjenje količine otpadne vode u odnosu na klasične načine guljenja. Osnova za kaustično guljenje je diferencijalno otapanje sastojaka stanica i tkiva.
.
Puferi i kontrola pH u namirnicama
Kako je većina namirnica kompleksan biološki materijal, one sadrže veliki broj sastojaka koji mogu sudjelovati u kontroli pH i puferskim sistemima. Tu se ubrajaju proteini, organske kiseline, te slabe anorganske kisele fosfatne soli. Mliječna kiselina i fosfatne soli, zajedno s proteinima, kontroliraju pH u tkivima animalnog porijekla. Polikarboksilne kiseline, fosfatne soli i proteini koriste se u tkivima biljnog porijekla, puferirajući utjecaj aminokiselina i proteina te utjecaj pH i soli na njihovu funkcionalnost.U slučajevima kada je potrebno promijeniti pH uglavnom je poželjno održavati ga pomoću puferskih sistema. Prirodno, to se postiže proizvodnjom mliječne kiseline u siru i fermentaciji ukiseljenog povrća. Osim toga, u slučajevima kada se u hranu i napitke dodaje veća količina kiseline, poželjno je smanjiti oštrinu kiselog okusa i povećati mekoću okusa primjenom neutralizirajućih aroma. Uglavnom se to postiže pomoću puferirajućih sistema u kojima prevladava sol ili slaba organska kiselina. Osnova uspostave kontrole pH u ovim sistemima je utjecaj iona, a sistem se uspostavlja kada dodana sol sadrži ion koji se već nalazi u postojećoj slaboj kiselini. Dodana sol odmah ionizira što rezultira smanjenom ionizacijom kiseline uz smanjenje kiselosti i stabilniji pH. Efikasnost pufera ovisi o koncentraciji puferirajućih materije. Kako je to smjesa nedisocirane kiseline i disocirane soli, pufer se opire promjeni pH. Na primjer, dodavanje relativno velike količine jake kiseline, poput HCl, u sistem octena kiselina – natrij acetat, uzrokovat će reakciju vodikovih iona sa acetat ionima te će se povećati udio slabo disocirane octene kiseline, a pH će ostati relativno stabilan. Na sličan način dodatak NaOH uzrokuje reakciju hidroksilnih iona s vodikovim ionima čime se stvaraju neutralne molekule vode.
Literatura
Spisak korišćene literature možete naći u Literatura – Hemija hrane.