Autor: Jelena Vulić
.
Hemijski sastav
Energetska vrednost cvekle je dosta visoka: 100 grama jestivog dela ima 154kJ (36kcal) (Ilić, 2009). Ona ima najveći sadržaj šećera od svog povrća, a niskokalorična je. Šećer koji je prisutan u cvekli, nalazi se u obliku koji organizam mnogo lakše apsorbuje. Ovaj šećer daje snagu i energiju i izvor je vitalnosti za ljudski organizam.
Tabela 3 : Sadržaj šećera u cvekli (Rodríguez-Sevilla et al., 1999):
| Šećer | Sadržaj(g/100g sirovine) |
| Fruktoza | 0,13 |
| Glukoza | 0,48 |
| Saharoza | 6,68 |
| Ukupni šećeri | 7,14-7,30 |
Sadržaj lipida u cvekli prikazan je u tabeli 4.
Tabela 4 : Sadržaj lipida u cvekli (Fineli, 2008)
| Vrste lipida | Sadržaj u 100g uzorka |
| Ukupne masne kiseline (g) | 0,2 |
| Ukupne zasićene masne kiseline (g) | <0,1 |
| Ukupne, monozasićene cis masne kiseline (g) | <0,1 |
| Ukupne, polizasićene masne kiseline (g) | 0,2 |
| Masne kiseline 18:2 cis, cis n-6 (linolna kiselina) (mg) | 131 |
| Masne kiseline 18:3, n-3 (α-linolna kiselina) (mg) | 22 |
| Ukupni steroli (mg) | 17,1 |
Sadržaj proteina u cvekli se kreće oko 1,3% (Vračar, 2001). „Zemljani“ ukus cvekle potiče od prisutnog geosmin-a. Različitim programima uzgoja cvekle, mogu se dobiti sorte sa niskim sadržajem geosmin-a i time prijatnijeg ukusa.
Vitaminski sastav cvekle je vrlo bogat. U cvekli je najzastupljeniji vitamin A (30mg), vitamin C (10mg) i u malim količinama vitamini B1, B2, B3 i B12 (Vračar, 2001). Ovo povrće ima čitav spektar minerala koji su neophodni čoveku za život i optimalno funkcionisanje: kalijum, natrijum, fosfor, kalcijum, magnezijum, gvožđe, fluor, sumpor, jod, brom, litijum, rubidijum, cezijum i stroncijum.
Tabela 5 : Sadržaj vitamina u cvekli (Fineli, 2008)
| Vitamini | Sadržaj u 100g uzorka |
| Vitamin A (μg) | 0,6 |
| Vitamin E (mg) | <0,1 |
| Vitamin K (μg) | 3,0 |
| Vitamin C | 10,0 |
| Folna kiselina (HPLC) (μg) | 150,0 |
| Niacin (mg) | 0,4 |
| Riboflavin (mg) | 0,05 |
| Tiamin (B1) (mg) | 0,05 |
| Piridoksin (mg) | 0,05 |
| Karotenoidi (μg) | 11,4 |
Tabela 6.: Sadržaj mineralnih materija u cvekli (Vračar, 2001)
| Mineralne materije | Sadržaj (mg/100g) |
| K | 260 |
| Na | 65,3 |
| P | 38 |
| Ca | 29 |
| Mg | 1,2 |
| Fe | 0,6 |
Betanin, pigment koji se nalazi u korenu cvekle i daje mu crvenu boju, suzbija viruse koji se javljaju uz prehladu, deaktivira bakterije i podstiče njihovo izbacivanje iz organizma. Ovaj pigment se u industriji koristi kao prehrambena boja (za pojačavanje boje sosova, dezerta, džemova, sladoleda, žitarica itd.).
Tabela 7.: Sadržaj betalaina u delovima korena cvekle (mg/g SM) (Kujala et al., 2002)
| Deo biljke | Betanin | Vulgaksantin I i II | Izobetanin |
| Pokožica | 3,8-7,6 | 1,4-4,3 | 1,2-3,1 |
| Meso | 2,9-5,2 | 1,5-4,0 | 0,02-0,4 |
Visoka koncentracija vlakana u cvekli omogućava pražnjenje creva i sprečava opstipaciju, i uopšte, dobra je za ceo digestivni trakt. Dovoljno je da pojesti 5 srednjih glavica cvekle da bi se zadovoljile dnevne potrebe organizma za vlaknima ( 30g/dan ).
Tabela 8.: Sadržaj dijetetskih vlakana u cvekli (Vollendorf &Marlett, 1993)
| Komponenta | (g/100g) |
| SM | 12,3 |
| Ukupna dijetetska vlakna (AOAC) | 2,5 |
| Ukupna dijetetska vlakna (Uppsala) | 2,1 |
| Nerastvorljiva dijetetska vlakna (Uppsala) | 1,4 |
| Rastvorljiva dijetetska vlakna (Uppsala) | 0,7 |
| Rastvorljiva dijetetska vlakna | |
| Hemiceluloza | 2,3 |
| Pektin | 3,6 |
| Nerastvorljiva dijetetska vlakna | |
| Hemoceluloza | 4,2 |
| Celuloza | 5,7 |
| Pektin | 1,5 |
| Lignin | 0,2 |
.
Slobodni radikali i antioksidanti
Pigmenti cvekle imaju snažno antioksidativno dejstvo.
Slobodni radikali su atomi, joni i molekuli koji sadrže jedan ili više nesparenih elektrona, koji, kada prestanu da kruže oko jezgra atoma, postaju prilično „agresivni“ i oštećuju sve na svom putu. Nastaju homolitičkim raskidanjem kovalentnih veza u organskim molekulima ili prenosom jednog elektrona na molekul (jon).
Slobodni radikali mogu nastati:
- fotolizom,
- termolizom (sagorevanjem ili zagrevanjem),
- elektromagnetnom radijacijom (dejstvom X- ili γ- zračenja),
- redoks reakcijama,
- hemijskim procesima (najčešće reakcijom kiseonika i slobodnih radikala) (Chimi, 1991).
Slobodnoradikalske reakcije su lančane i započinju ih inicijatori. Početni stadijum ovih reakcija je faza inicijacije u toku koje nastaje nova slobodnoradikalska vrsta. Sledeća faza je faza propagacije u toku koje slobodni radikali nastali u prvoj fazi reaguju sa novim molekulima gradeći nove slobodne radikale. Poslednja faza, tj. završetak ovih lančanih reakcija je faza terminacije, kada nastaju neaktivni, neradikalski proizvodi (Tumbas, 2005).
U normalnim uslovima, nastajanje slobodnih radikala je u ravnoteži sa endogenim antioksidativnim sistemom odbrane ćelije. Pri nekontrolisanom stvaranju slobodnih radikala, može se premašiti antioksidativni kapacitet ćelije i tada nastaje tzv. oksidativni stres. To je stanje u kome je ravnoteža između prooksidanata i antioksidanata u ćeliji, pomerena u pravcu prooksidanata (Halliwell, 1985).
Slobodni radikali „uzimajući“ elektrone od susednih molekula, oštećuju ćelije i tkiva i zbog toga izazivaju mnoge patološke promene i obolenja: artritis, pankreatitis,hemolitičku anemiju, Parkinsonovu bolest, Kronovu bolest itd. Dovode do oštećenja proteina, lipida, ugljenih hidrata i DNK (Diplock i sar., 1998).
Malo je poznato da je kiseonik potencijalni čovekov neprijatelj. On je većini organizama na Zemlji neophodan za život, ali zbog svoje velike reaktivnosti, sklon je stvaranju slobodnih radikala i toksičnih kiseoničnih vrsta (ROS). Zbog toga, u našem organizmu postoji kompleksna mreža antioksidativnih metabolita i enzima, koji zajedno sprečavaju formiranje reaktivnih metabolita ili ih uklanjaju pre nego što oštete vitalne funkcije ćelije (www. en. wikipedia.com). To su endogeni antioksidansi (npr. ženski polni hormoni, koenzim Q, fermenti superoksida dizmutaze, katalaze, glutatjon itd.).
Iako naše telo stvara mnogo antioksidanata, to nije dovoljno da se ono izbori sa svim slobodnim radikalima. Zbog toga je neophodno antioksidante unositi i sa hranom (egzogeni). Antioksidansima su bogati: voće i povrće, žitarice, mahunarke, orasi (tabela 3).
Tabela 9. Antioksidansi i namirnice u kojima se nalaze
| Antioksidant | Hrana sa visokim sadržajem antioksidansa |
| Vitamin C | voće i povrće |
| Vitamin E (tokoferol) | ulje povrća |
| Polifenoli (flavonoidi, resveratrol) | kafa, čaj, soja, čokolada, origano, crveno vino, cimet, maslinovo ulje |
| Karotenoidi (likopen, karoteni) | voće i povrće |
Antioksidansi su supstance koje, u malim koncentracijama, usporavaju ili sprečavaju reakcije oksidacije kojima se stvaraju slobodni radikali (Halliwell,1994).
Mišljenje mnogih naučnika je, da su antioksidanti redukujuća sredstva koja i sama lako oksiduju i zato uspešno dovode do terminacije lančanih reakcija oksidacije. Postoje razni mehanizmi njihovog delovanja:
- deluju kao hvatači („skevindžeri“) slobodnih radikala,
- daju elektrone i redukuju neka jedinjenja,
- razgrađuju hidroperokside lipida koji su nastali u fazi propagacije,
- eliminišu dejstvo singletnih oblika kiseonika,
- inhibiraju neke enzime,
- pokazuju sinergetske efekte (Weber, 1996).
Prema načinu delovanja, antioksidanti se dele na:
- primarne,
- sekundarne,
- tercijarne.
Prema poreklu, dele se na:
- sintetske,
- prirodne.
Prema funkciji koju obavljaju u organizmu:
- preventivni,
- kao hvatači slobodnih radikala,
- antioksidantni enzimi koji obnavljaju strukturu ćelije,
- adaptivni.
U najvažnije prirodne antioksidanse se ubrajaju vitamin C i E, vitamin B3 u formi niacina, vitamini B2 i B6, koenzim Q, β-karoten, likopen, lutein, fenolna jedinjenja.
.
Polifenoli
.
Fenolna jedinjenja cvekle
Cvekla je bogat izvor fenolnih jedinjenja, galne, p-kumarinske, ferulne, vanilinske, p-hidroksi benzoeve i siringinske kiseline (Pirjo Mattila i sar., 2006).
Fenolna jedinjenja ili polifenoli, su najrasprostranjeniji sekundarni metaboliti biljaka koji se zbog svoje arome i lekovitosti upotrebljavaju u medicini, farmaceutskoj, kozmetičkoj i prehrambenoj industriji.
Polifenoli čine najbrojniju grupu jedinjenja sa visokom antioksidativnom aktivnošću. Ova jedinjenja u svom sastavu imaju bar jedan aromatični prsten sa jednom ili više hidroksilnih grupa. Šematski se opšta struktura polifenola može prikazati na sledeći način:
Slika 1. Rezonantna stabilizacija radikala koji nastaje iz fenola
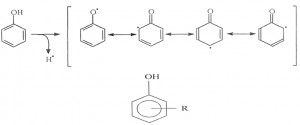
Smatra se, da je antioksidativna aktivnost, posledica sposobnosti polifenola da budu donori vodonikovih atoma i da pri tome uklanjaju slobodne radikale uz formiranje manje reaktivnih fenoksil – radikala (slika 1). Ovi radikali su stabilniji zbog delokalizacije elektrona i postojanja više rezonantnih formi. Što je stabilnost nastalog fenoksil radikala veća, to je veća mogućnost nastanka rekombinantnih reakcija, koje dovode do terminacije slobodnoradikalskih reakcija.
U zavisnosti od strukture, fenolna jedinjenja u biljkama mogu nastati:
- putem šikimske kiseline,
- acetogeninskim putem,
- mešovitim biosintetskim putem.
Najvažniji put biosinteze aromatičnih jedinjenja u višim biljkama je ciklus šikimske kiseline. Ova kiselina je izolovana iz biljaka familije Illicium, mnogo godina pre nego što je otkrivena njena uloga u metabolizmu. Tokom ciklusa šikimske kiseline sintetišu se aromatične aminokiseline (L-fenilalanin, L-tirozin i L-triptofan), esencijalni kofaktori (folna kiselina), važne strukturne materije (lignin) i veliki broj sekundarnih metabolita (fenilpropanoidi, alkaloidi, antibiotici i dr.). Deaminacijom nastalih aminokiselina nastaju cimetna kiselina i sva jedinjenja koja imaju strukturu fenil-propana. Složenim hemijskim reakcijama iz ovih proizvoda nastaju i druge grupe fenolnih jedinjenja.
Postoje različite klasifikacije polifenola. U tabeli 10 navedena je klasifikacija fenolnih jedinjenja na osnovu broja konstitutivnih ugljenikovih atoma osnovnog skeleta fenola.
Tabela 10. Podela fenolnih jedinjenja
| Osnovni skelet | Klasa | Jedinjenje |
| C6 | Prosti fenoli | Katehol,hidrohinon,rezorcinol |
| Benzohinoni | ||
| C6-C1 | Fenolne kiseline | p-hidroksibenzoeva kiselina |
| C6-C2 | Fenilsirćetne kiseline | p-hidroksifenilsirćetna |
| C6-C3 | Cimetne kiseline | Kafena kiselina, ferulna kiselina |
| Fenilpropeni | Eugenol, miristicin | |
| Kumarini | Umbeliferon, eskuletin, skopolin | |
| Hromoni | Eugenin | |
| C6-C4 | Naftohinoni | Juglon |
| C6-C1-C6 | Ksantoni | Mangostin, magniferin |
| C6-C2-C6 | Stilbeni | Razveratrol |
| Antrahinoni | Emodin | |
| C6-C3-C6 | Flavonoidi | |
| Flavoni | Apigenin, luteolin,sinensitin,nobiletin, izosinensitin,tangeretin,diosmin | |
| Flavonoli | Kvarcetin, kamferol | |
| Flavonol glikozidi | Rutin | |
| Flavanoli | Dihidrokvarcetin i dihidrokamferol glikozidi | |
| Flavanoni | Hesperidin, naringenin | |
| Flavanon glikozidi | Hesperidin, neohesperidin, narirutin, naringinin, eriocitrin | |
| Antocijanini | Glikozidi peralgonidina, peonidina, delfinidina, petunidina, cijanidina | |
| Katehini | Katehin, epikatehin, galokatehin, epigalokatehin | |
| Halkoni | Floridžin, arbutin, halkonarigenin | |
| (C6-C3)2 | Lignini | Pinorezinol |
| (C6-C3-C6)2 | Biflavonoidi | Agatisflavon, amentoflavon |
Fenolna jedinjenja nisu ravnomerno rasprostranjena u biljnim tkivima. Najznačajniji izvori fenolnih jedinjenja, a time i izvori antioksidanata su razni napici (zeleni i crni čaj, crno vino, pivo, kafa, voćni sokovi), kakao, crna čokolada, lešnik, badem, kikiriki i drugo jezgrasto voće, šljive, grožđe, jabuke, borovnice, brusnice, maline, kupine, masline, soja, integralne žitarice, brokoli, paštrnak, kupus, luk, celer itd. U tabeli 5 prikazana je zastupljenost fenolnih jedinjenja u prirodnim proizvodima.
Tabela 11. Prirodni izvori fenolnih jedinjenja (Sakakibara, 2003)
| Klasa | Primer | Izvor |
| Prosti fenoli | Hlorogenska,kafena, galna, ferulna kiselina | veoma rasprostranjeni, naročito u krtolastom povrću |
| Glikozidi flavona i flavonola | Apigenin, luteolin, kvercetin, kamferol, glikozidi miricetina | lisnato povrće |
| Aglikoni flavona i flavonola | Apigenin, luteolin, galangin | peršun, celer, prokelj i biljke |
| Izoflavoni | Genistein, daidžein i njihovi glikozidi | soja |
| Flavanoni | Naringenin i glikozidi hesperidina | citrus voće |
| Katehini | Epigalokatehin, epigalokatehingalat, galokatehin | čajevi i kakao |
| Antocijani | Pelargonidin, cijanidin, malvidin,delfinidin | obojeni prirodni proizvodi: patlidžan,borovnica,crna soja |
| Antrahinoni | Emodin, hrizofanol, rein | krušina, sena, aloja |
Od ukupne količine unetih fenolnih jedinjenja u organizam, jedna trećina su fenolne kiseline, a dve trećine flavonoidi.
.
Betalaini
Visok sadržaj betalaina u cvekli je posebno značajan, jer ova supstanca služi kao polazna osnova u sintezi holina, koji predstavlja jednu od najaktivnijih supstanci u organizmu. Betalaini su glavni pigmenti cvekle.
.
Klasifikacija i biosinteza
Termin betalaini (lat. beta=beet) usvojen je 1968. za žute i crvene N-heterociklične pigmente ploda kruške i cvekle, koji su do tada greškom zvani flavocijani ( betaksantini, grčki : xanthos= žuto ) i azotni antocijani (betacijani, grčki : kyaneous=plavo). 1963. i 1964., betanin i indiksantin su bili prvi betacijanin i betaksantin čija je struktura određena iz cvekle ( Beta vulgaris L. ) i ploda kruške ( Opuntia ficus indica [L.] Mill ). Godinu dana kasnije betalainska kiselina je predložena za njihov zajednički biosintetički prekursor.
Betalaini predstavljaju azotne derivate betalainske kiseline i podeljeni su na crveno-ljubičaste betacijane i žuto-narandžaste betaksantine. Zanimljivo je da antocijani i betalaini isključuju jedni druge – nisu nikada nađeni u istoj biljci zajedno. Vogt je izneo dokaz da su se betalaini pojavili posle antocijana na skali evolucije. Ove činjenice ukazuju na to da antocijani i betalaini zamenjuju jedni druge u određenim funkcijama u biljnom tkivu kao što su polarno privlačenje, antioksidativni potencijal i zaštita od ultraviolentne ( UV ) svetlosti. Obe klase pigmenata imaju put šikimske kiseline, vodeći do tirozina ( betalaini ) ili fenilalanina ( antocijani ).
Boja antocijana je od narandžaste ( pelargonidin ), crvene ( cijanidin ) do plave ( delfinidin ), betalaini se mogu podeliti u žuto-narandžaste ( betaksantin ) i crveno-ljubičaste strukture ( betacijani ). Takođe, biljke koje sadrže betalaine mogu sadržati i leukoantocijane i proantocijane, ali uz nedostatak enzimske mogućnosti da generiše 3-hidroksi-antocijane.
Put betalaina se deli u tri glavna pravca, prvi vodi do cyclo-dopa i njegovih glukozida. Posle cepanja dopa, 4,5-secodopa ili 2,3-secodopa je proizveden, kasnije dovodi do izomera betalaminske kiseline muscaflavin, tipičan za Hygrophorus, Hygrocybe i Amanita rodove. Tipična putanja viših biljaka se nastavlja 4,5-secodopa strukture uglavnom dajući betalaminsku kiselinu, ključni prekursor za većinu betacijana i betaksantina. Još uvek nije objašnjeno da li je kondenzacija aminokiselina ili amina sa betalaminskom kiselinom u betaksantine spontana ili je kontrolisana enzimima. Za betacijane, aktuelna istraživanja treba da pokažu da li je cyclo-dopa glikolizovan pre ili posle kondenzacije sa betalainskom kiselinom.
.
Fizičke i hemijske karakteristike
Betalaini su biljni pigmenti u vakuolama. Imaju hidrofilnu prirodu. Voda je najbolji rastvarač, a blago su rastvorljivi u etanolu i metanolu. U poređenju sa antocijanima, betalaini su polarniji, što se ispoljava kraćim retencionim vremenom (RP-HPLC) i nižom rastvorljivošću u alkoholnim rastvorima. Razlika u polarnosti se koristi za razdvajanje antocijana od betalaina na RP-18 kertridžu solid-phase ekstrakcijom.
Koeficijenti ekstinkcije antocijana su manji nego betalaina (11300 L/mol cm – 29000 L/mol cm) za najčešće antocijan-3-glikozide, dok je za betaksantine i betacijane 48000 L/mol cm i 60000 L/mol cm.
Betalaini su osetljivi na prisustvo metala, sumpor-dioksida, svetlost, visoku vodenu aktivnost, enzimsku aktivnost, pH i povišene temperature. Betaksantini su najstabilniji na pH 5,5 do 7. Betacijani su najstabilniji na pH 5-6, a betalaminska kiselina ostaje netaknuta na pH 9. Degradacija betalaina pod drugim pH vrednostima nije istražena.
.
Rasprostranjenost, stabilnost i modifikacija posle berbe
Betalaini su N-heterociklični pigmenti, rastvorljivi u vodi. Nalaze se u vakuolama. Njihov prekursor je betalaminska kiselina koja se sastoji od 1,7-diazoheptametin sistema. Betalaminska kiselina može da se kondenzuje sa cyclo-dopa dajući betanidin, prekursor aglikon crvenih betacijana. Betanidin može biti glikolizovan i/ili acilovan, dajući 29 struktura. Zbog stereoizomerizma na C15 njihov broj je udvostručen, izuzev za neobetanin (14, 15-dehidrobetanin) koji nema hiralni centar na C15.
Žuti analozi, betaksantini, sastoje se od betalaminske kiseline sa aminokiselinama ili aminima, rezultujući 26 struktura.
.
Distribucija, prirodna funkcija i delovanje
Betalaini se javljaju u 13 familija Caryophyllales i nikada se ne javljaju u istoj biljci istovremeno sa antocijanima. Oni se nalaze u nekim rodovima viših gljiva (Amanita, Hygrocybe, Hygrophorus). U jestivim biljkama se betalaini javljaju u ograničenoj količini u odnosu na antocijane.
.
Stabilnost i modifikacija posle branja
Mogu se razlikovati dve grupe faktora koji utiču na stabilnost betalaina. Prvi su endogeni faktori, kao što su biljni enzimi polifenoloksidaze, peroksidaze i ß-glukozidaze. Ostali faktori koji utiču na boju betalaina su ekstrakcioni medijum, temperatura, kiseonik i pH.
pH vrednost
Betalaini su najstabilniji u oblasti pH 3 do 7. Betalaini cvekle su najstabilniji na pH 5,5 do 6. Vrednost pH ispod 3 uzrokuju gubitak boje. U baznoj sredini, betalaini će se raspasti na njihove biosintetičke prekursore, betalaminsku kiselinu i cyclo-dopa (betacijane) ili amino komponente (betaksantine), dalje vodeći ka potpunom izbeljivanju. Betacijani su postojaniji u baznoj sredini, a betaksantini u neutralnoj pH sredini. Betalaini su pogodniji za niskokiselu hranu, kao što su mlečni i mesni proizvodi, kao i sladoled.aw vrednost
Kao i kod ostalih prirodnih boja, aktivnost vode je štetna za za stabilnost boje. Povećanjem sadržaja vode biće povećana i mobilnost komponenti hrane i rastvoljivost kiseonika, vodeći ka nestabilnosti betalaina. Kao posledica ovog, betalaini se mogu koristiti za voćna punjenja, kremove, instant proizvode, kao što su supe. Priprema boje je obično koncentrovanjem ili sušeno raspršivanjem do najmanje 65ºBx, da bi se obezbedila maksimalna stabilnost tokom transporta i skladištenja.
Endogeni i egzogeni enzimi
Uloga ß-glukozidaze na betalaine je jasna, dok polifenoloksidaze i peroksidaze je manje razjašnjena. Glikozidi betacijana se mogu rascepati u odgovarajuće aglikone, koji mogu kasnije biti nestabilni i dalje se mogu oksidovati.
Mikroorganizmi korišćeni za denitrifikaciju i uklanjanje šećera pre koncentrovanja ili fermentacije mlečnom kiselinom može biti treći izvor cepanja glikozida. Polifenoloksidaze i peroksidaze bilnog tkiva mogu biti inaktivirane jedino toplotom. Period između gnječenja i filtriranja soka treba da bude što kraći. Peroksidaze utiču na stabilnost betalaina formiranjem radikala, a polifenoloksidaze oksiduju aglikone betalaina i prateće fenole. Konačno, zakišeljavanje predstavlja odličan način za dezaktiviranje endogenih enzima.
Metalni joni
Metalni joni koji uzrokuju gubitak boje betalaina su Sn2+, Al 3+, Ni2+ , Cr 2+, Fe 2+, Fe 3+ i Cu 2+ (poslednja dva su najštetnija). Metalni joni mogu biti sa ploda, zemljišta ili mašina za obradu. Na prvi izvor se teško može uticati, dok se na drugi može uticati snažnim pranjem. Potencijalna kontaminacija ne bi trebala da bude problem, kada se koristi odgovarajuća oprema. Da bi se smanjila oksidacija metalnim jonima, preporučuje se upotreba limunske kiseline za zakišeljavanje i kao helirajući agens u proizvodnji pigmenata.
Kiseonik
Kiseonik je osnova za sve gore pomenute oksidativne enzime. Katalizuje metalom uzrokovanu oksidaciju i direktno utiče na stabilnost betalaina, posebno izvan optimuma pH. Obogaćivanje azotom se može preporučiti, ali retko se primenjuje. Rastvorljivost kiseonika u vodi je poboljšana kada je snižena temperatura vode. Oksidacija se odvija sporije u hladnom okruženju, poboljšavajući celokupnu retenciju pigmenata.
Svetlost
U biljnom tkivu, betalaini kao UV-filteri brzo absorbuju svetlosnu energiju. Betalaini se degradiraju kada su izloženi svetlosti, posebno u prisustvu kiseonika i van optimalnog opsega pH. Proizvodnja i skladištenje treba da budu izvedeni bez izlaganja svetlosti. Proizvodi koji se prodaju u providnom pakovanju, treba da budu testirani u odgovarajućim uslovima. Takođe, treba uzeti u obzir da izlaganje proizvoda svetlosti zagreva proizvod. Zanimljivo, uticaj svetlosti se jedino meri ispod 25ºC.
Temperatura
Temperatura je najpresudniji faktor stabilnost betalaina. Termička obrada je poželjna za inaktivaciju enzima i sprečavanje mikrobiološkog kvarenja. Preparatima iznad pH 4,3, kao što su cvekla ili plod kruške se dodaje limunska kiselina do pH 4, da bi se sprečio uticaj uslova sterilizacije. Pasterizacija ispod 100ºC je dovoljna da bi se postigla mikrobiološka stabilnost. Degradacija betalaina je iznad 30ºC, gubitak boje tokom obrade je neizbežan (Socaciu, 2007).
.
Literatura
- Chimi, H., Cillard, J., Cillard, P., Rahmani, M., JAOCS, 68, 307-312, 1991.
- Diplock, A. T., J. L. Charleaux, at al., Functional Food Science and Defence Against ROS, Nutr. 80, 1998.
- Halliwell, B., Gutteridge, J. M. C., Free Radicals in Biology and Medicine, Press, Oxford, 1985.
- Halliwell, B., Nut. Rev., 52, 253-265, 1994.
- Halliwell, B., Chirico, S. Lipid peroxidation: Its mechanism, measurement and significance, American Journal of Clinical Nutrition, Vol 57, 715S-724S, Copyright, 1993.
- http://sr.wikipedia.org
- http://www.en.wikipedia.com
- Ilić, Z., Fallik, E., Đurovka, M., Martinovski, Đ., Trajković, R.: Fiziologija i tehnologija čuvanja povrća i voća, 2007.
- Ilić, Z., Fallik, E., Dardić, M.: Berba, sortiranje, pakovanje i čuvanje povrća, 2009.
- Kader, A. Adel,: Postharvest Technology of Horticultural Cropsb, Agriculture and Natural Resources, 2002.
- Lazic, B., Djurovka, M., Markovic, V., Ilin, Z.: Povrtarstvo. Univerzitet u Novom Sadu, Poljoprivredni fakultet, 1998.
- Niketić-Aleksić, G. (1982): Tehnologija voća i povrća, Poljoprivredni fakultet, Beograd.
- Niketić-Aleksić Gordana: Tehnologija voća i povrća, Naučna knjiga, Beograd, 1998.
- Pirjo Mattila, Jarkko Hellström,: Phenolic acids in potatoes, vegetables, and some of their products, Journal of Food Composition and Analysis 20, pp. 152–160, 2007.
- Pravilnik o kvalitetu proizvoda od voća, povrća, pečurki i pektinskih preparata, Sl. list SFRJ 1/79.
- Sakakibara, H., Honda, Y., Nakagawa, S., Ashida, H., Kanazawa, K., Simultaneous Determination of all Polyphenols in Vegetables, Fruits and Teas, J. Agric. Food Chem., 51, 571-581, 2003.
- Socaciu C., Food colorants, Chemical and functional properties, 2007.
- Tumbas, V.,Antioksidativna i biološka aktivnost ekstrakata biljaka iz familije Luminaceae, Magistarski rad, Tehnološki fakultet, Novi Sad, 2005.
- Tytti S. Kujala, Jyrki M. Loponen, Karel D. Klika, Kalevi Pihlaja., Phenolics and Betacyanins in Red Beetroot (Beta vulgaris) Root: Distribution and Effect of Cold Storage on the Content of Total Phenolics and Three Individual Compounds, J. Agric. Food Chem., 48 (11), pp 5338–5342, 2000.
- Vereš, M.: Osnovi konzervisanja namirnica, Poljoprivredni fakultet, Naučna knjiga, 1991.
- Vračar, Lj.: Priručnik za kontrolu kvaliteta svežeg i prerađenog voća, povrća, pečurki i bezalkoholnih pića, Tehnološki fakultet, Novi Sad, 2001.
- Vračar LJ., Tepić A., Letić A, Palinka M.: Sušenje maline postupkom liofilizacije, Jugosl. voćar. Vol. 38. br. 147–148 (2004/3–4), 209–214.
- Weber, P.A. Benedich and human health- a review of recent data relevant to human requirements. Int. J. Vitamin Nutr. Res. 66-69, 1996