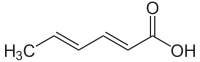Autor: Ivana Bakočević, magistar tehnologije
E200 SORBINSKA KISELINA
Strukturna formula:
| Definicija | Prirodno organsko jedinjenje. Sredstvo za konzervisanje; sprečava rast gljivica i buđi (Clostridium Botulinum), ali ne i bakterija (npr. u sirevima). |
| Dobijanje | Tradicionalno se dobija kondenzacijom malonske kiseline i trans-butenala. Takođe, može se pripremiti od izomera heksadienske kiseline, dobijene nikl-katalizovane reakcije alil-hlorida, acetilena i ugljen-monoksida. Procenjeno je da se proizvodi oko 30.000t godišnje. Može se dobiti ekstrakcijom iz voća. |
| Hemijsko ime | Sorbinska kiselina |
| Trans,trans-2,4-heksadienska kiselina | |
| EINECS | 203-768-7 |
| Hemijska formula | C6H8O2 |
| Molekulska masa | 112,12 |
| Određivanje | Najmanje 99,0 % u izračunato u odnosu na bezvodnu supstancu |
| Osobine | Bezbojne iglice ili beo lako pokretljiv prašak slabog karakterističnog mirisa koji ne menja boju zagrevanjem 90 min na 105oC. Ima blago kiseli ukus. |
| Upozorenje | U pojedinim slučajevima može izazvati alergiju (iritacija kože). Osobe koje boluju od pseudoalergija, astme ili neurodermitisa trebale bi izbegavati namirnice konzervisane sorbinskom kiselinom. |
| Identifikacija | |
| A. Temperatura topljenja | 133oC – 135oC, posle sušenja 4 h u vakuum eksikatoru iznad sumporne kiseline |
| B. Spektrofotometrija | Maksimum na 254 2 nm u izopropanolu (1 : 4 000 000) |
| V. Pozitivno ispitivanje za dvostruke veze | |
| G. Temperatura sublimacije | 80oC |
| Čistoća | |
| Sadržaj vode | Najviše 0,5 % (Karl Fischer-ova metoda) |
| Sulfatni ostatak | Najviše 0,2 % |
| Aldehidi | Najviše 0,1 % (kao formaldehid) |
| Arsen | Najviše 3 mg/kg |
| Olovo | Najviše 5 mg/kg |
| Živa | Najviše 1 mg/kg |
| Teški metali (kao Pb) | Najviše 10 mg/kg |
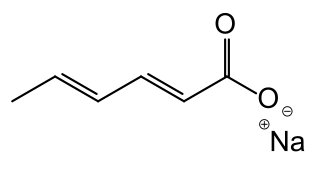
E 202 KALIJUM-SORBAT
Strukturna formula:
| Definicija | Dobija se neutralizacijom kalijum-hidroksida sa nezasićenom sorbinskom kiselinom. Koristi se za sprečavanje razvoja buđi i gljivica u sirevima, jogurtu, vinu, suhomesnatim proizvodima, osvežavajućim napitcima, voćnim sokovima, pekarskim proizvodima… |
| Hemijsko ime | Kalijum-sorbat |
| Kalijumova so trans, trans-2,4-heksadienske kiseline | |
| EINECS | 246-376-1 |
| Hemijska formula | C6H7O2K |
| Molekulska masa | 150,22 |
| Određivanje | Najmanje 99,0 % izračunato u odnosu na osušenu supstancu |
| Osobine | Beo kristalan prašak koji ne menja boju zagrevanjem 90 min na 105oC |
| Identifikacija | |
| A. Temperatura topljenja sorbinske kiseline izolovane zakiseljavanjem bez rekristalizacije | 133oC – 135oC posle sušenja 4 h u vakuum eksikatoru iznad sumporne kiseline |
| B. Pozitivna ispitivanja za kalijum i za dvostruke veze | |
| Čistoća | |
| Gubitak sušenjem | Najviše 1,0 % (105oC, 3 h) |
| Aciditet ili alkalitet | Najviše 1,0 % (kao sorbinska kiselina ili K2SO3) |
| Aldehidi | Najviše 0,1 % (kao formaldehid) |
| Arsen | Najviše 3 mg/kg |
| Olovo | Najviše 5 mg/kg |
| Živa | Najviše 1 mg/kg |
| Teški metali (kao Pb) | Najviše 10 mg/kg |
E 203 KALCIJUM-SORBAT
| Definicija | Kalcijumova so sorbinske kiseline, koristi se za konzerviranje iste grupe namirnica kao kod E200, 201, 202. |
| Hemijsko ime | Kalcijum-sorbat |
| Kalcijumove soli trans,trans-2,4-heksadienske kiseline | |
| EINECS | 231-321-6 |
| Hemijska formula | C12H14O4Ca |
| Molekulska masa | 262,32 |
| Određivanje | Najmanje 98,0 % izračunato u odnosu na osušenu supstancu |
| Osobine | Beo, fin kristalan prašak koji ne menja boju zagrevanjem 90 min na 105oC |
| Identifikacija | |
| A. Temperatura topljenja sorbinske kiseline izolovane zakiseljavanjem bez rekristalizacije | 133oC – 135oC, posle sušenja 4 h u vakuum-eksikatoru iznad sumporne kiseline |
| B. Pozitivna ispitivanja za kalcijum i za dvostruke veze | |
| Čistoća | |
| Gubitak sušenjem | Najviše 2,0 % posle sušenja 4 h u vakuum eksikatoru sa sumpornom kiselinom |
| Aldehidi | Najviše 0,1 % (kao formaldehid) |
| Fluoridi | Najviše 10 mg/kg |
| Arsen | Najviše 3 mg/kg |
| Olovo | Najviše 5 mg/kg |
| Živa | Najviše 1 mg/kg |
| Teški metali (kao Pb) | Najviše 10 mg/kg |
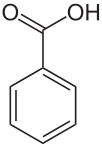
E 210 BENZOEVA KISELINA
Strukturna formula:
| Definicija | Najjednostavnija organska aromatična kiselina. Dobija se sintetski. Koristi se kao prehrambeni konzervans protiv kvasaca, buđi i nekih bakterija. Dozira se izmedju 0,05-0,1%. U napitcima može da reaguje sa vitaminom C, gradeći benzen. |
| Hemijsko ime | Benzoeva kiselina |
| Fenilkarboksilna kiselina | |
| EINECS | 200-618-2 |
| Hemijska formula | C7H6O2 |
| Molekulska masa | 122,12 |
| Određivanje | Najmanje 99,5% u izračunato u odnosu na bezvodnu supstancu |
| Osobine | Beo kristalan prašak |
| Identifikacija | |
| A. Temperatura topljenja | 121,5oC – 123,5oC |
| B. Pozitivana ispitivanja za sublimaciju i za benzoat | |
| Čistoća | |
| Gubitak sušenjem | Najviše 0,5 % posle sušenja 3 h iznad sumporne kiseline |
| pH | Oko 4 u vodenom rastvoru |
| Sulfatni ostatak | Najviše 0,05 % |
| Hlorovana organska jedinjenja | Najviše 0,07 % izraženo kao hloridi tj. 0,3 % izraženo kao monohlorbenzojeva kiselina |
| Supstance koje lako oksidišu | Doda se 1,5 ml sumporne kiseline u 100 ml vode, zagreje do ključanja i doda u kapima 0,1 N KMnO4 do pojave ružičaste boje postojane 30 s. 1,000 g uzorka rastvori se u zagrejanom, gore opisanom rastvoru, i titrira 0,1 N rastvorom KMnO4 do ružičaste boje postojane 15 s. Najviše 0,5 ml može da bude utrošeno za titraciju. |
| Supstance koje lako karbonizuju | Hladan rastvor 0,5 g benzojeve kiseline u 5 ml 94,5 % – 95,5 % sumporne kiseline nije intenzivnije obojen od poredbenog rastvora koji sadrži 0,2 ml kobalt(II)-hlorida TP1, 0,3 ml gvožđe(II)-hlorida TP2, 0,1 ml bakar(II)-sulfata TP3 i 4,4 ml vode. |
| Policiklične kiseline | Prvi precipitat dobijen frakcionim zakiseljavanjem neutralizovanog rastvora benzojeve kiseline mora da ima istu temperaturu topljenja kao benzojeva kiselina. |
| Arsen | Najviše 3 mg/kg |
| Olovo | Najviše 5 mg/kg |
| Živa | Najviše 1 mg/kg |
| Teški metali (kao Pb) | Najviše 10 mg/kg |
Izvori
http://en.wikipedia.org/wiki/E_number
http://www.food-info.net/
http://mentarihannover.blogspot.com/2011/04/what-is-halaal-part-1.html
http://www.medicinasportiva.ro/dr.drosescu/en/food_additives.html#supplements
http://www.ukfoodguide.net/enumeric.htm
http://www.earthways.co.uk/enumbers.html
http://curezone.com/foods/enumbers.asp
M.V. Piletić, B.Lj.Milić, S.M.Đilas, Organska hemija II, Prometej 1993.
http://www.reading.ac.uk/foodlaw/additive.htm